Добавление - аминокислота
Cтраница 1
 |
Фрагмент реплицирующейся ДНК хромосомы из разрушенных ядер Dro. [1] |
Добавление аминокислот после голодания вызывало инициацию репликации с лаг-периодом, равным всего 6 мин. [2]
Более удобно инициировать эту реакцию добавлением аминокислоты непосредственно перед началом реакции. [3]
Биологическая ценность белков может быть увеличена добавлением лимитирующей аминокислоты или внесением компонента с ее повышенным содержанием. Так, биологическая ценность белка пшеницы может быть повышена приблизительно в два раза добавлением 0 3 - 0 4 % лизина, белка кукурузы - 0 4 % лизина и 0 7 % триптофана. [4]
Максимальное созревание окраски с симазином достигается при нагревании его с пиридином на кипящей водяной бане в течение 2 ч, тогда как для дирена оптимальное время реакции составляет 20 мин при комнатной температуре. Оптимальные результаты для симазина достигаются в том случае, если конечная концентрация NaOH составляет 1 г-экв / л, а пиридина - 12 % по объему. Как и для дирена, интенсивность окраски увеличивается при добавлении аминокислоты - гликоколя, хотя максимум поглощения при этом остается тем же самым. Поэтому для получения возможно более интенсивной окраски пиридиновый реактив насыщают гликоколем. [5]
 |
Одномерная хрома-тограмма для обнаружения ФТГ-аспарагиновой кислоты и ФТГ-глутаминовой кислоты.| Двумерная хроматограмма смеси, содержащей по 0 5 цг ФТГ-аминокислот, МФТГ. [6] |
Остаток смешивают с 250 л л буферной смеси триэтиламин - уксусная кислота ( см. реактивы) и 250 л л ацетонового раствора фенилизотиоцианата ( что соответствует 6 1л ФИТЦ), тщательно перемешиваемую пробу при герметичном затворе оставляют на 2 5 час в водяной бане при 25; затем отфильтровывают раствор с применением в течение 15 мин водоструйного насоса, после чего на 12 час оставляют в глубоком вакууме над пятиокисью фосфора. HGl-ледяная уксусная кислота); полученный раствор выдерживают 6 час в водяной бане при 25 и растворитель и кислоту удаляют, как описано выше, над КОН. Остаток содержит ФТГ-аминокислоты; для хроматографического сравнения проводят параллельный опыт без добавления аминокислоты. ФТГ-производные цистеина и цистина по описанной методике получить нельзя. Для определения этих аминокислот перед гидролизом следует провести окисление надмуравьиной кислотой; в этом случае после гидролиза получают цистеиновую кислоту и из нее более или менее удовлетворительно - ФТТ-производное. [7]
 |
Одномерная хрома-тограмма для обнаружения ФТГ-аспарагиновой кислоты и ФТГ-глутаминовой кислоты. J.| Двумерная хроматограмма смеси. [8] |
ФИТЦ), тщательно перемешиваемую пробу при герметичном затворе оставляют на 2 5 час в водяной бане при 25; затем отфильтровывают раствор с применением в течение 15 мин водоструйного насоса, после чего на 12 час оставляют в глубоком вакууме над пятиокисью фосфора. Осадок ( фенилтиокарбамилпроизводные аминокислот) растворяют в 100 и. HCl-ледяная уксусная кислота); полученный раствор выдерживают 6 час в водяной бане при 25 и растворитель и кислоту удаляют, как описано выше, над КОН. Остаток содержит ФТГ-аминокислоты; для хроматографического сравнения проводят параллельный опыт без добавления аминокислоты. ФТГ-производные цистеина и цистина по описанной методике получить нельзя. Для определения этих аминокислот перед гидролизом следует провести окисление надмуравьиной кислотой; в этом случае после гидролиза получают цистеиновую кислоту и из нее более или менее удовлетворительно - ФТГ-производное. [9]
Это заставляет считать, что в окислении гидроксиль-ных ионов принимает участие или фотовозбужденный пигмент фотосистемы 2 или непосредственно с ним связанная неизвестной природы оксидоредуктаза. Дело в том, что в модельных системах фотовозбужденный хлорофилл не может отнимать электроны от веществ, имеющих Е 0 выше 0 1 в. Недавно Кутюрину ( 1967) удалось значительно усилить электроно-акцепторные свойства хлорофилла добавлением аминокислот щелочного характера ( лизина, аргинина, гистидина) к водно-ацетоновому раствору хлорофилла. Образующийся комплекс хлорофилл а - аминокислота при освещении приобретает Е 0 0 8 или даже 0 9 в. По мнению Кутюрина, хлорофилл, связанный с остатками этих аминокислот в пигмент-белковом комплексе хлоропластов, в фотоокисленном состоянии способен окислять воду. [10]
В связи с этим уместно заметить, что ранее некоторые исследователи ( Mayer, Krehl, 1948; Stoewsand, Scott, 1961; Nir, Ascarelli, 1966) наблюдали у животных, содержащихся на диете с дефицитом витамина А, ускорение мобилизации витамина А из депо по мере повышения количества белка в корме, тогда как другие авторы ( Deshrnukh, Ganguly, 1964) параллельно увеличению степени дефицита протеинов в диете обнаружили замедление мобилизации и расходования витамина в организме. Метаболическая реализация витамина А находится в прямой зависимости от скорости роста животных, на которую влияет не только количество белка в пище, но и его качественный состав. К примеру, у крыс, получавших корм с 18 % казеина, отмечено более быстрое потребление запасов ретинола, чем у крыс, получавших вместо животного белка аналогичное количество пшеничной клейковины или зеина. В свете этих данных, возвращаясь к результатам нашего опыта, следует допустить, что добавление физиологических количеств лизина и метиони-на к клейковине ( при этом сохраняется дефицит одного треонина) обусловливает повышенный расход ретинола, что усиливает его недостаточность в организме и ускоряет развитие гиповитаминоза А. Иными словами, добавление аминокислот влияет на метаболизм ретинола подобно увеличению количества полноценного белка в рационе и способствует развитию в этих условиях более выраженного нарушения азотистого обмена, чем при дефиците двух или трех незаменимых аминокислот и витамина. [11]
Получить ауксотрофные мутанты, способные накапливать конечные продукты неразветвленных цепей биосинтеза, например L-аргинин, невозможно. В таких случаях приходится отбирать мутанты с частично нарушенной регуляцией биосинтеза, что позволяет получить повышенный выход конечного продукта. Такие мутанты известны под названием регуляторных; их отбирают по устойчивости к аналогам аминокислот или же средин ревертантов ауксотрофов. В основе использования аналогов-аминокислот лежит их сходство с природными аминокислотами. Они ингибируют рост бактерий, но этот эффект может быть уменьшен путем добавления соответствующей природной аминокислоты. Таким образом, аналоги выступают в роли искусственных, работающих по принципу обратной связи, ингибиторов-ферментов, обеспечивающих биосинтез природных аминокислот. Появление мутантов, устойчивых к этим ложным ингибиторам, означает, что регуляторные ферменты соответствующего пут № обмена становятся у них нечувствительными к аналогу. Так, серусодержащий аналог лизина 5 - ( 2-аминоэтил) - Ь - цистеин является у Brevibacterium flauum ложным, действующим по принципу обратной связи ингибитором аспартокиназы. Устойчивые к его действию мутанты вырабатывают фермент, который в 150 раз менее чувствителен к ингибированию по механизму обратной связи, чем фермент исходного штамма, и в результате продуцируют до 33 г / л лизина. [12]
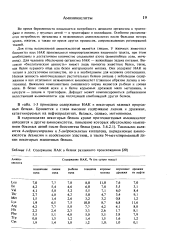 |
Содержание НАК в белках различного происхождения. [13] |
Для птиц незаменимой аминокислотой является глицин. Высокую биологическую ценность имеют лишь немногие животные белки, такие, как белок куриного яйца или белок материнского молока. Важными компонентами смешанного корма являются рыбная и соевая мука. В белке соевой муки и в белке кормовых дрожжей мало метионина, в кукурузе - лизина н триптофана. Дефицит может компенсироваться добавлением недостающей аминокислоты или подходящей комбинацией других белков. [14]
Страницы: 1