Добавление - избыток - осадитель
Cтраница 1
Добавление избытка осадителя и появление свободных хромат-ионов ведет к увеличению предельного тока, что обусловлено их восстановлением до хрома шпшсп степени окисления. Подобная кривая ( рис. 122, в) получается при титровании 8-оксихинолином цинка. При потенциале ртутно-капельного катода - 1 32 В полярографичсски активны оба взаимодействующих вещества. [1]
 |
Кривые, соответствующие. [2] |
Добавление избытка осадителя и появление свободных хромат-ионов ведет к увеличению предельного тока, что обусловлено восстановлением их до хрома низшей степени окисления. [3]
В нейтральном растворе при добавлении избытка осадителя осадок растворяется. Реакции мешают нитрат-ионы [687] и катионы, образующие осадки с реагентом, большинство из которых, правда, растворяется в соляной кислоте. Метод может быть использован для открытия галлия в сфалерите [1246] в присутствии Zn, Cd, Fe, Mn, Pb, Hg, Sn, In; Cu, Co, Ni, Mg, Ca не мешают обнаружению галлия. [4]
Как видно из расчета, при добавлении избытка осадителя растворимость осадка настолько уменьшается, что потерей его вследствие растворимости при данных условиях можно пренебречь. Однако следует иметь в виду, что чрезмерный избыток осадителя не только не понижает, а, наоборот, повышает растворимость осадка. Это объясняется явлением солевого эффекта и способностью осадка превращаться в растворимые комплексные соединения и кислые соли. [5]
Так, в качественном анализе нередко первоначально выпадающий осадок снова растворяется при добавлении избытка осадителя. [6]
Так, при качественном анализе нередко встречаются случаи, когда первоначально выпадающий осадок снова растворяется при добавлении избытка осадителя. [7]
Однако осаждение в таких условиях становится неполным, поэтому в конце осаждения растворимость осадка тем или иным способом понижают, например, растворимость осадка BaSC4 добавлением избытка осадителя. В случае осаждения Са2 в виде СаС2С4 кислотность раствора уменьшают добавлением NI-UOH по каплям, при этом отложение осадка происходит вследствие роста ранее образовавшихся кристаллов. Осадок СаС2О4 - Н2О, полученный таким способом, хорошо отфильтровывается, а при осаждении из нейтрального или щелочного раствора он проходит через поры фильтра. [8]
Признаком того, что при взаимодействии солей органических кислот и солей редкоземельных металлов образуется комплексное соединение, считалось образование осадка и последующее его растворение при добавлении избытка осадителя. Подтверждением того, что здесь возникает комплексное соединение, являлась отрицательная реакция с обычными осадителями: ферроцианидом, аммиаком, щелочью, оксалатом, фторидом. [9]
При соответствующих количествах полисахарида и осадителя образующийся комплекс выпадает немедленно при смешении растворов. При добавлении избытка осадителя образуется гидрофобная коллоидная суспензия, которая в отсутствии других электролитов не отделяется центрифугированием от раствора. Частички комплекса имеют положительный заряд вследствие адсорбции небольшого количества положительных ионов аммониевого основания. Двухвалентные катионы ( Mg, Са) в присутствии одновалентных анионов оказывают стабилизирующее действие и не коагулируют суспензию даже при нагревании. Двухвалентные анионы обладают сильным коагулирующим действием. При добавке небольшого количества Na2SOi происходит коагуляция солей при комнатной температуре через несколько минут. [10]
В электролитическую ячейку переносят аликвотную часть раствора и разбавляют в два раза этиловым спиртом. При добавлении избытка осадителя электропроводность раствора увеличивается. По кондуктометрической кривой находят количество миллилитров оксалата лития, вступивших в реакцию, и проводят расчеты, как описано в гл. [11]
Раствор металлов разбавляют до 400 мл, подкисляют 40 мл серной кислоты ( 1: 1), охлаждают до 10 - 15, хорошо перемешивая, прибавляют по каплям осадитель до коагуляции желтого осадка и просветления жидкости над ним. Последнюю проверяют на полноту осаждения добавлением избытка осадителя: появление сразу исчезающего белого осадка нитрозофенилгидроксиламина указывает на полноту осаждения титана. Для осаждения необходим значительный избыток реактива. [12]
Как показывают эксперименты, пз трех разновидностей выделения полимера из раствора основными являются только две: застудневание и распад на два жидких слоя. Выделение полимера в виде осадка наблюдается при добавлении избытка осадителя как для систем, образующих студни, так и для систем с разделением на два жидких слоя. По внешнему виду осадки в обоих случаях мало разнятся между собою. [13]
Для предотвращения выпадения слишком мелких осадков необходимо: а) вести осаждение из разбавленных растворов солей разбавленным раствором осадителя; б) приливать раствор осадителя медленно, по каплям, постоянно перемешивая раствор стеклянной палочкой; в) повышать растворимость образующегося осадка, ведя осаждение из горячего раствора или прибавляя тот или иной реактив, повышающий растворимость образующегося соединения. Эта повышенная растворимость должна быть в дальнейшем понижена охлаждением раствора или добавлением избытка осадителя, или каким-либо другим способом. [14]
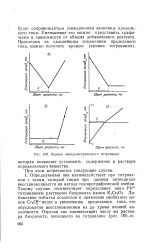 |
Кривые амперометрического титрования. [15] |
Страницы: 1 2