Малое количество - серная кислота
Cтраница 1
Малые количества серной кислоты заметно не улучшают окраску и стабильность. Нужно ожидать, что эффективность серной кислоты зависит от крекинг-бензина. В других случаях удовлетворительный результат в отношении цвета и стабильности может быть достигнут применением меньших или больших количеств реагента. [1]
При малых количествах серной кислоты исследуемую каплю вместе с уксуснокислым кальцием или 1 / 0-ным раствором СаС12 концентрируют на водяной бане. После охлаждения рассматривают под микроскопом. Если во время охлаждения капля совершенно высохнет, то перед наблюдением остаток увлажняют дыханием. Под микроскопом видны палочки или иглы гипса. [2]
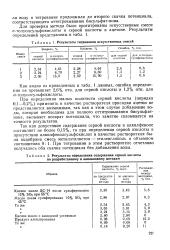 |
Результаты титрования искусственных смесей.| Результаты определения содержания серной кислоты по разработанному и анилиновому методам. [3] |
При определении малых количеств серной кислоты ( порядка 0 1 - 0 2 %) применять в качестве растворителя присадки ацетон не представляется возможным, так как в этом случае добавление воды, которая необходима для полного оттитровывания бисульфат-иона, вызывает возврат потенциала, что заметно сказывается на точности результатов. [4]
Если отделение было проведено с малым количеством серной кислоты, то фильтрат от вольфрамовой кислоты можно выпарить в платиновой чашке, удалить большую часть серной кислоты выпариванием, остаток смыть аммиаком во взвешенный платиновый тигель, выпарить, прокалить и взвесить. При значительном количестве молибденовой кислоты всегда надежнее осадить молибден в виде сернистого, как это было указано выше. [5]
Уменьшение октанового числа не велико при малых количествах серной кислоты, но значительно при употреблении 25 кг и больше серной кислоты на 1 м3 бензина. [6]
Осадок сернистых металлов растворяют в азотной кислоте, выпаривают с малым количеством серной кислоты, обрабатывают остаток водой, почти полность ю нейтрализуют едким натром ( приготовленным из металлического натрия. К фильтрату прибавляют еще некоторое количество цианистого калия и немного разбавленного раствора сернистого калия. Серебро и кадмий выпадают в виде сернистых металлов. В цианистом фильтрате разрушают цианистый калий выпариванием со смесью азотной и серной кислот. Остаток от выпаривания нагревают с некоторым количеством соляной кислоты, осаждают медь сероводородом и определяют ее в виде полусернистой меди или в виде окиси. [7]
Гидролиз уксусного ангидрида протекает почти мгновенно при действии воды в присутствии малых количеств серной кислоты. Метод пригоден для определения уксусного ангидрида в присутствии больших количеств уксусной кислоты. [8]
С, содержавшая около 1 5 % сульфидной серы, окислена гетерогенно-эмульсионным методом с добавкой малых количеств серной кислоты ( см. ниже, стр. [9]
Ими установлено, что благоприятными условиями для образования сс-ионона являются: применение низких ( от - 40 до - 60 С) температур, малых количеств серной кислоты и небольшая продолжительность реакции циклизации. [10]
В поиске лучшего решения было разработано так называемое самоокрашивающееся анодирование, известное в действительности уже очень давно, но дополненное новыми изобретениями, позволяющими образовывать стойкие анодные цветные покрытия на промышленном уровне. Для этого необходимы ванны, состоящие из органических кислот и малого количества серной кислоты, отвечающие, в основном, потребностям, строительной архитектуры, предпочитающей черный цвет, разные бронзовые оттенки и некоторые более светлые цвета. Окончательный вид зависит не только от самой ванны, но и от марки алюминиевого сплава. [11]
 |
Устройство конденсационного или клапан следует уста горшка. навливать на трубопроводе. [12] |
Требования к качеству жидкого хлора определяются как уело виями его последующей переработки ( особенно в хлоропродукты) так и условиями хранения и транспортирования. Отсюда вытекает необходимость максимального содержания С12 в сжиженном газе и его минимальной влажности, малого количества серной кислоты треххлористого азота и других примесей, приносимых из исходно го хлоргаза. [13]
 |
Поляризационные кривые в 3 5 н. растворах ( NH4 2SO4 и H2SO4 при 7 С.| Поляризационные кривые в 4 5 н. растворах ( NH4 2SO4 и H2SO4 при. [14] |
Необходимо, однако, отметить, что утверждение Смита и Хугленда о преимущественном участии иона 8О - в образовании иона S2Ol - противоречит данным об ионном составе растворов серной кислоты, полученным с помощью раманов-ских спектров. По-видимому, участие ионов SO - в электрохимической реакции, протекающей с образованием S2Os -, возможно преимущественно в растворах сульфатов, содержащих малые количества серной кислоты, где концентрация сульфат-ионов действительно велика. [15]
Страницы: 1 2