Добавление - сильное основание
Cтраница 1
Добавление сильного основания, например ОН -, значительно усиливает гидролиз гидрати-рованных катионов вследствие связывания протонов, отщепляемых в реакции гидролиза. Подобные реакции простых катионов в основных растворах обычно протекают по одному из трех перечисленных ниже типов, хотя возможны и отдельные исключения. [1]
При добавлении сильного основания или сильной кислоты изменение величин концентрации уксусной кислоты и ее соли может быть заметным, но даже при изменении отношения Стся / Ссозт в 10 раз логарифм этой величины изменится всего лишь на единицу. [2]
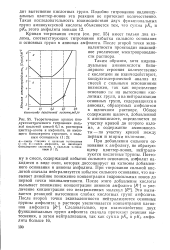 |
Теоретические кривые кон-дуктометрического титрования сильной кислотой смесей 0 1 н. растворов цвиттер-ионов и амфолита, не имеющего биполярного строения, с сильным основанием ( 1. 2. [3] |
При добавлении сильного основания к амфолиту, не образующему цвиттер-ионов, нейтрализуются кислотные группы. Поэтому в смеси, содержащей избыток сильного основания, амфолит находится в виде соли, которая диссоциирует на катионы добавленного основания и анионы амфолита. При титровании сильной кислотой сначала нейтрализуется избыток сильного основания, что вызывает линейное понижение концентрации гидроксильных ионов до первой точки эквивалентности. Это вызывается реакцией вытеснения слабых кислотных групп амфолита. [4]
Стабильные кислые соли аминов разлагают добавлением сильных оснований ( карбоната натрия, едкого натра); амин извлекают последующей перегонкой. Реакция этаноламинов с цианистым водородом дает, вероятно, сложные неорганические соли. [5]
Для них не требуется наличия активирующих групп или добавления сильных оснований. На реакцию не влияет присутствие таких групп, как алкил, алкокси, арил и СОО -, однако группы Me2N, О - и NO2 оказывают влияние. [6]
Следовательно, буферная смесь противодействует также изменению ее рН при добавлении сильных оснований. Способность буферного раствора сохранять неизменной концентрацию ионов водорода - называется буферным действием. [7]
Таким образом, при добавлении к раствору KtAn какой-либо сильной кислоты возникает буферный раствор слабой кислоты и ее соли, а при добавлении сильного основания - буферный раствор слабого основания и его соли. [8]
Их получают из растворов солей при добавлении сильных оснований. [9]
Нетрудно вычислить изменения концентрации ионов водорода, происходящие при добавлении сильного основания к раствору сильной кислоты, если можно считать кислоту нацело диссоциированной. В любой момент нейтрализации концентрация ионов водорода сц равна концентрации ненейтрализованной сильной кислоты. Если а - начальная концентрация кислоты в эквивалентах на 1 л, а Ъ - количество добавленного основания в эквивалентах на 1 л в любой момент, то концентрация ненейтрализованной кислоты равна а - b эквивалентов в 1 л и равна концентрации ионов водорода. [10]
От добавления к буферному раствору сильной кислоты или сильного основания концентрации кислоты и соли меняются. Поэтому высокая концентрация кислоты НА еще недостаточна для того, чтобы раствор оказывал буферное действие при добавлении сильного основания. [11]
В растворах многоосновных кислот ( оснований), так же как и в смеси кислот ( оснований), диссоциация более слабых электролитов подавлена более сильными. Поэтому при добавлении сильного основания к смеси кислот оттит-ровывается прежде всего сильная и только, когда оставшегося количества ее не хватает для подавления диссоциации более слабой, начинается ее титрование. В противном случае скачки фенолфталеином ( ФФ) и метиловым оран-сливаются. [12]
Рассчитайте растворимость ацетата серебра в чистой воде и количество выпадающей в осадок окиси серебра ( если осадок образуется), учитывая образование комплексов ацетата серебра ( см. табл. VIII. При каком рН начинается выпадение окиси серебра из насыщенного раствора ацетата серебра при добавлении сильного основания. [13]
Хансен и Ружичка, которые сконструировали электрод с воздушным промежутком ( [40]; см. также гл. Процесс идет в две ступени: сначала при рН 7 мочевина превращается в NH, а при добавлении сильного основания происходит образование аммиака. Гильбо и Тарп [42 ] создали условия для протекания реакции в одну ступень посредством химически иммобилизованной уреазы, которая удерживалась на дне сосуда с исследуемым образцом. [14]
Другими словами, для данной общей концентрации компонентов буферного раствора максимальная буферная емкость имеет место при равной концентрации обоих компонентов. Для определенного соотношения СА / СВ буферная емкость пропорциональна общей концентрации С. Очень важно понять, что при добавлении к буферному раствору сильной кислоты или основания концентрации обоих компонентов - СА и Св - изменяются. Следовательно, наличие высокой концентрации кислоты Л еще недостаточно для того, чтобы раствор оказывал буферное действие при добавлении сильного основания и наоборот. Уравнение ( 3 - 71), содержащее произведение двух концентраций, наглядно подтверждает это. [15]
Страницы: 1