Определенное весовое количество
Cтраница 3
Количество ( весовое или в случае газа, объемное) растворенного вещества, содержащееся в определенном весовом количестве ( или в определенном объеме) раствора, называется концентрацией раствора. [31]
Количество ( весовое или, в случае газа, объемное) растворенного вещества, содержащееся в определенном весовом количестве ( или в определенном объеме) раствора, называется концентрацией раствора. [32]
ЭКВИВАЛЕНТОВ ЗАКОН - один из законов химии, устанавливающий, что элементы всегда соединяются между собой в определенных весовых количествах, соответствующих их эквивалентам химическим. [33]
ЭКВИВАЛЕНТОВ ЗАКОН - один из основных законов химии, устанавливающий, что элементы всегда соединяются между собой в определенных весовых количествах, соответствующих их химическим эквивалентам. [34]
Концентрация весовых растворов характеризуется числом граммов растворенного вещества в определенном весовом количестве или объеме раствора; молярных растворов - числом молей растворенного вещества в определенном весовом количестве или объеме раствора или растворителя. [35]
Обоим требованиям удовлетворяет система оценки активности, в которой основной величиной является общая активность, определяемая как число молекул, реагирующих в единицу времени на поверхности определенного весового количества катализатора, например 1 г. Общая активность легко может быть вычислена, если определены соответствующие кинетические константы. [36]
Исследование свойств разбавленных растворов неэлектролитов показало, что величины понижения давления пара, повышения температуры кипения и понижения температуры замерзания обусловлены только числом растворенных частиц в определенном весовом количестве данного растворителя и не зависят от природы растворенного вещества. В этом заключается сущность законов Рауля. [37]
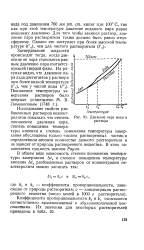 |
Давление пара воды и раствора. [38] |
Исследование свойств разбавленных растворов неэлектролитов показало, что степень понижения давления пара, степень повышения температуры кипения и степень понижения температуры замерзания обусловлены только числом растворенных частиц в определенном весовом количестве данного растворителя и не зависят от природы растворенного вещества. В этом заключается сущность законов Рауля. [39]
После растворения пробы исследуемой смолы в подходящем растворителе и прибавлении смеси соляной кислоты с растворителем определяют количество связанной кислоты, что позволяет установить число эпоксидных групп, содержащихся в определенном весовом количестве смолы. При рас - чете следует учитывать свободную кислоту или свободное основание, которое может присутствовать в пробе. [40]
Закон постоянства состава означает, что каждое Определенное вещество, независимо от того, как оно получено, всегда состоит из одних и тех же элементов, соединенных друг с другом в строго определенных весовых количествах. Например, вода всегда состоит из двух элементов: водорода и кислорода, причем на 2 вес. [41]
Классически для определения молекулярных весов таких веществ - применяются два физико-химических метода: а) криоскопический метод, состоящий в измерении понижения точки замерзания соответствующего растворителя при добавлении к нему небольшого, но определенного весового количества неизвестного вещества в качестве растворенного вещества, не образующего твердых растворов, б) эбулиоскопический метод, состоящий в измерении точки кипения соответствующего растворителя при добавлении небольшого количества неизвестного вещества, которое по сравнению с растворителем является нелетучим. [42]
После растворения пробы исследуемой смолы в подходящем растворителе ( диоксан) и прибавления смеси соляной кислоты с диоксаном определяют по разности количество связанной кислоты, что позволяет установить число эпоксидных групп, содержащихся в определенном весовом количестве смолы. При расчете, разумеется, учитывают свободную кислоту или свободное основание, могущие присутствовать в пробе. [43]
В одной из своих последующих работ Лавуазье по этому же поводу указывал: Я предполагаю, что мне дана соль, и ни ее кислота, ни основание мне неизвестны; я ввожу в реторту определенное весовое количество ее, приливаю серной кислоты и перегоняю; в приемнике у меня оказывается азотная кислота, а в реторте я нахожу сернокалиевую соль, отсюда я заключаю, что данная мне для исследования соль была селитрой. [44]
Предварительные опыты могут быть выполнены с использо ванием небольших трубок ( со слоем ионита от нескольких мл до 25 мл) или же с помощью контактного процесса, в котором определенный объем раствора приводится в соприкосновение с определенным весовым количеством ионообменной смолы. Если применяются различные концентрации металлических ионов, то могут быть построены изотермы адсорбции Фрейндлиха, которые весьма полезны при предварительной оценке ионообменных смол и процессов. [45]
Страницы: 1 2 3 4