Заметное количество - аммиак
Cтраница 1
 |
Схема объемно-весового реактора.| Изотермы адсорбции азота и окиси углерода на тренированном катализаторе. [1] |
Заметные количества аммиака на исследуемом контакте образуются лишь при температуре 190 С. [2]
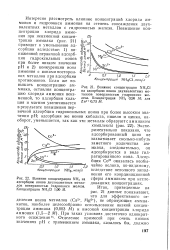 |
Влияние концентрации NH4C1 на адсорбцию ионов двухвалентных металлов поверхностью гидроокиси же. [3] |
Экспериментально показано, что адсорбированный цинк не захватывает сколько-нибудь заметного количества аммиака, следовательно, он адсорбируется в виде гид-ратированного иона. [4]
При этом из раствора выделяются водород и азот, что свидетельствует о восстановлении растворителя и о каталитическом его разложении. Было пэказано, что в полученных растворах содержатся заметные количества аммиака. [5]
Реакции окисления гидразина в щелочной среде не были изучены столь подробно, как соответствующие реакции в кислой среде. При добавлении окиси или сульфата двухвалентной меди к щелочным растворам гидразина получаются заметные количества аммиака, однако азид водорода в этих условиях не образуется. Кольтгофф [33, 127] впгрвые указал, что гидразин в щелочной среде количественно окисляется перманганатом до азота. [6]
Так как аммиак при высоких температурах разлагается, то на первый взгляд может показаться, что следовало бы поддерживать в реакторе достаточно низкую температуру, при которой аммиак не разлагается. Но к сожалению, сколько бы вы не держали смесь трех объемов водорода и одного объема азота при комнатной температуре, заметных количеств аммиака не образуется. [7]
Тщательно взбалтывают в течение получаса и смесь оставляют на 12 час. Так как под действием щелочи в эфирный экстракт переходит заметное количество аммиака, для его удаления жидкость 2 мин продувают воздухом при помощи резиновой груши. Метод Келлера прост и удобен при массовых анализах. [8]
Основное свойство катализаторов состоит в том, что после участия в реакции они остаются, как правило, химически неизменными. Подтверждением этого может служить, например, синтез аммиака из азота и водорода. Если смешать азот и водород, то никакими усилиями - ли повышением давления до 1000 ат, ни применением высоких температур - не удается получить заметного количества аммиака. Но этот процесс стал возможным благодаря использованию в качестве катализатора обычного железа с небольшими добавками окислов калия, алюминия, кальция, кремния, называемых промоторами или активаторами. [9]
Основное свойство катализаторов состоит в том, что после участия в реакции они остаются, как правило, химически неизменными. Подтверждением этого может служить, например, синтез аммиака из азота и водорода. Если смешать азот и водород, то никакими усилиями - ни повышением давления до 1000 ат, ни применением высоких температур - не удается получить заметного количества аммиака. Но этот процесс стал возможным благодаря использованию в качестве катализатора обычного железа с небольшими добавками окислов калия, алюминия, кальция, кремния, называемых промоторами или активаторами. [10]
В системе производства карбамида циркулируют значительные объемы газов. Газы со стадии дистилляции и выпаривания, содержащие аммиак и диоксид углерода, уносят и некоторое количество карбамида. На рис. 1 - 2 приведены объемы основных потоков современного цеха производства карбамида мощностью 1000 т / сут4 Грануляцию карбамида производят в грануляционных башнях при охлаждении воздухом. На этой стадии вместе с воздухом также уносится заметное количество аммиака и карбамида. Все это приводит к необходимости создания на установках по производству карбамида многочисленных узлов абсорбции и десорбции аммиака и диоксида углерода. [11]
 |
Адсорбция ионов двухвалентных металлов поверхностью гидроксида железа. [12] |
На рис. 9 - 1 показано [11] влияние изменения концентрации хлорида аммония и гидроксида аммония на степень соосаждения двухвалентных металлов с гидроксидом железа. Повышение концентрации хлорида аммония при неизменной концентрации аммиака приводит к уменьшению адсорбции вследствие: 1) пониженной первичной адсорбции гидроксидных ионов при более низком значении рН и 2) конкуренции иона аммония с ионами посторонних металлов при адсорбции противоионов. Если же повышать концентрацию аммиака, оставляя концентрацию хлорида аммония неизменной, то адсорбция кальция и магния увеличивается в результате повышения первичной адсорбции гидроксидных ионов при более высоком значении рН; адсобрция же ионов кобальта, никеля и цинка, наоборот, уменьшается, так как эти металлы образуют с аммиаком комплексы. Экспериментально показано, что адсорбированный цинк не захватывает сколько-нибудь заметного количества аммиака, следовательно, он адсорбируется в виде гидратированного иона. Как было указано в разд. Предполагается, что образуются ферриты двухвалентных металлов. [13]
То же самое относится к процессу дегидратации гидрата гидразина с помощью окиси кальция. В этом случае дегидратирующее вещество и гидратированный продукт также нерастворимы в гидразине. Для получения удовлетворительного выхода гидразина требуется высокая температура, однако чрезмерное повышение ее может привести к разложению. Согласно данным Штелера [33], продукт, полученный при отгонке гидразина от окиси кальция при температурах, достигающих 150 С, содержит заметное количество аммиака. [14]
Страницы: 1