Общее количество - поглощенный кислород
Cтраница 1
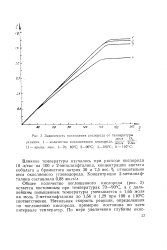 |
Зависимость поглощения кислорода от температуры. [1] |
Общее количество поглощенного кислорода ( рис. 2) остается постоянным при температурах 70 - 90 С, а с дальнейшим повышением температуры уменьшается с 1 65 моля на моль 2-метилнафталина до 1 56 и 1 29 при 100 и ЫО С соответственно. Начальная скорость реакции, определенная по поглощению кислорода, примерно постоянна во всем интервале температур. [2]
Графическое интегрирование этого уравнения позволяет определить общее количество поглощенного кислорода. [3]
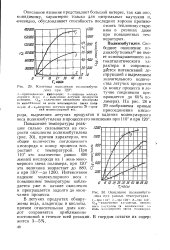 |
Окисление полиизобутилена при разных температурах. [4] |
Повышение температуры реакции сильно сказывается на ско - IZOO рости окисления полиизобутилена ( рис. 30), причем характерно, что общее количество поглощенного кислорода к концу процесса возрастает с температурой. Интенсивное падение молекулярного веса с повышением температуры наблюдается уже в начале окисления и прекращается задолго до окончания процесса. [5]
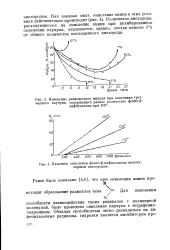 |
Изменение равновесного модуля при окислении трехмерного каучука, содержащего разное количество фенил-р-нафтиламина при 100.| Кинетика окисления фенил-р-нафтиламина молекулярным кислородом. [6] |
Количество кислорода, расходующегося на окисление амина при ингибированном окислении каучука, оказывается, однако, всегда меньше 3 % от общего количества поглощенного кислорода. [7]
Здесь величины, отмеченные простыми и двойными штрихами вверху, относятся соответственно к высшему и низшему окислам в момент времени t, a qx есть общее количество поглощенного кислорода. Таким образом, в момент времени t 0 значения g и также равны нулю. [8]
В табл. П-4 приведено сравнение продуктов окисления циркулирующим кислородом некоторых типов углеводородов при 110 С. Величины выражены в процентах от общего количества поглощенного кислорода. [9]
В течение 50 мин 0 45 ммолъ / л Na2S ( около 75 % от введенного количества) окисляется, затем количества образовавшегося и израсходованного сульфида меняются параллельно. На рис. 142 показаны скорости образования и расходования сульфида, а также общее количество поглощенного кислорода. Из рисунка видно, что скорости образования и расходования сульфида и скорость поглощения кислорода изменяются симбатно, а их максимумы совпадают во времени. Все это указывает на наличие между ними глубокой связи. Можно полагать, что окисление сульфида оказывает большое влияние на поглощение кислорода меркаптоуксусной кислотой. Представляется вполне вероятным, что автокаталитический характер реакции обусловлен присутствием сульфида. [10]
К числу очень немногих получивших известность примеров такого подхода относится работа Менона и др. [73], который обнаружил, что кислород, хемосорбированный при комнатной температуре на рении, в отличие от хемосорбированного на платине кислорода не восстанавливается водородом. Поэтому приняв, что катализатор Pt-Re / irj - AlaOs содержит только отдельные частицы чистой платины и чистого рения ( но не их сплава), можно по общему количеству поглощенного кислорода определить суммарную металлическую поверхность, а по доле хемосорбированного кислорода, взаимодействующего с водородом при комнатной температуре согласно уравнению ( 12) - поверхность платины; тогда разность соответствует поверхности рения. Однако, если на поверхности находится сплав, этого простого объяснения недостаточно, так как необходимо знать и учитывать любые реакции, протекающие также на этой части поверхности. Температура реакции не единственный параметр, который изменяется при переходе от одного металла к другому, при этом может меняться и стехиометрия хемосорбции. В качестве примера отметим разную стехиометрию реакции хемосорбированного кислорода с водородом при комнатной температуре на платине и на никеле, которая отражена уравнениями ( 12) и ( 14) соответственно. [11]
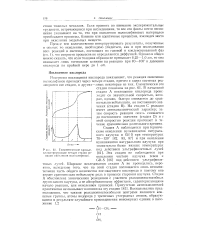 |
Гипотетические кривые, иллюстрирующие четыре стадии реакции окисления полиолефинов. [12] |
На стадии С реакция имеет автокаталитический характер; за тем скорость реакции опять снижается до постоянного значения ( стадия D) и с этой скоростью реакция протекает в течение сравнительно длительного времени. Эта стадия не наблюдается при окислении чистого каучука гевеи и GR-S [86] под действием ультрафиолетовых лучей. Широкие исследования стадии А не проводились, вероятно, вследствие того, что на этой стадии поглощается лишь незначительная часть общего количества поглощенного кислорода и поэтому она играет сравнительно небольшую роль в процессе старения каучука. Стадия А обусловлена химическими реакциями с участием реакционноспособных групп самого каучука, а не абсорбционными эффектами, характеризующими начало реакции, или окислением примесей. [13]
Недавно Скейт и Ван Гофф [38] путем очень тонкого эксперимента, при котором газообразный кислород напускался на слегка восстановленные образцы ТЮ2, SnO2 или ZnO, действительно обнаружили оба типа парамагнитных частиц О2 и О по их сигналам ЭПР. Следовательно, этот сигнал следует приписать одноатомным парамагнитным частицам СГ. В этом исследовании было найдено, что общее количество парамагнитных частиц составляет около 1 % от общего количества поглощенного кислорода. [14]
Страницы: 1