Добавление - апротонный растворитель
Cтраница 1
Добавление апротонных растворителей, константа автопрото-лиза которых теоретически стремится к нулю, к протолитическим приводит к уменьшению A s смешанных растворителей. С другой стороны, апротонные растворители характеризуются низкими значениями диэлектрической проницаемости, поэтому НСЮ4 и ( C2H5) 4N OH в среде смешанных растворителей диссоциированы меньше, чем в среде протолитических растворителей. Это приводит к тому, что в одних случаях смеси апротонных растворителей с протолитическими растворителями имеют относительную шкалу кислотности больше, чем у протолитических растворителей, а в других случаях - меньше. Так, добавление апротонного растворителя к спиртам, имеющим небольшие шкалы кислотности, приводит к увеличению, а добавление к кетонам и нитрилам, которые обладают большими шкалами кислотности, приводит к уменьшению относительной шкалы кислотности. [1]
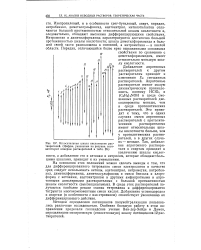 |
Относительная шкала кислотности растворителей. ( Цифры, указанные на рисунке, соответствуют номерам растворителей в 26. [2] |
Добавление апротонных растворителей к другим растворителям приводит к изменению ES смешанных растворителей. Апротонные растворители имеют малую диэлектрическую проницаемость, поэтому НС1О4 и ( CgHshNOH в среде смешанных растворителей диссоциированы меньше, чем в среде протолитических растворителей. Это приводит к тому, что в одних случаях смеси апротонных растворителей с протолити-ческими растворителями имеют относительные шкалы кислотности больше, чем у протолитических растворителей, а в других случаях - меньше. [3]
Добавление апротонных растворителей, константа автопрото-лиза которых теоретически стремится к нулю, к протолитическим приводит к уменьшению Ks смешанных растворителей. С другой стороны, апротонные растворители характеризуются низкими значениями диэлектрической проницаемости, поэтому НСЮ4 и ( СгНбЬ ОН в среде смешанных растворителей диссоциированы меньше, чем в среде протолитических растворителей. Это приводит к тому, что в одних случаях смеси апротонных растворителей с протолитическими растворителями имеют относительную шкалу кислотности больше, чем у протолитических растворителей, а в других случаях - меньше. Так, добавление апротонного растворителя к спиртам, имеющим небольшие шкалы кислотности, приводит к увеличению, а добавление к кетонам и нитрилам, которые обладают большими шкалами кислотности, приводит к уменьшению относительной шкалы кислотности. [4]
Добавление апротонных растворителей к другим растворителям приводит к изменению Es смешанных растворителей. Апротонные растворители имеют малую диэлектрическую проницаемость, поэтому НС1О4 и ( C2H5) sNOH в среде смешанных растворителей диссоциированы меньше, чем в среде протолитических растворителей. Это приводит к тому, что в одних случаях смеси апротонных растворителей с протолитическими растворителями имеют относительные шкалы кислотности больше, чем у протолитических растворителей, а в других случаях - меньше. Так, добавление апротонного растворителя к спиртам приводит к увеличению шкалы кислотности, а добавление его к кетонам и нитрилам, которые обладают большими шкалами, приводит к их уменьшению. [5]
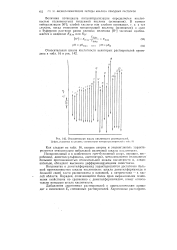 |
Относительная шкала кислотности растворителей. Цифры, указанные на рисунке, соответствуют номерам растворителей и 16. [6] |
Добавление апротонных растворителей к протолитическим приводит к изменению Es смешанных растворителей. [7]
Понижение концентрации протонов в двойном электрическом слое замедляет скорость протонизации, приводящей к образованию-пропионитрила, и благоприятствует образованию адиподинитрила. Добавление апротонных растворителей также снижает протонодонор-ную способность среды. В том случае если концентрация протонов очень мала, анионы начинают десорбироваться в объем раствора, инициируя образование олигомера. [8]
При добавлении апротонных растворителей, с одной стороны, происходит уменьшение Ks среды, что ведет к увеличению относительной шкалы кислотности, с другой стороны, наблюдается уменьшение относительной шкалы кислотности в присутствии апротонных растворителей. Следовательно, в зависимости от того, какой из указанных выше факторов оказывает наибольшее влияние, относительная шкала кислотности смешанных растворителей либо увеличивается, либо уменьшается по сравнению со шкалой кислотности исходных растворителей. [9]
При добавлении апротонных растворителей к протолитическим, с одной стороны, происходит уменьшение Ks среды, что ведет к увеличению относитель-ной шкалы кислотности, с другой стороны, наблюдается уменьшение диэлектрической проницаемости среды, что ведет к уменьшению относительной шкалы кислотности, так как потенциалы полунейтрализации НСЮ4 и ( HsbNOH при титровании их в присутствии апротонных растворителей сближаются. Следовательно, в зависимости от того, какой из указанных выше факторов оказывает наибольшее влияние, относительная шкала кислотности смешанных растворителей либо увеличивается, либо уменьшается по сравнению со шкалой кислотности протолитических растворителей. [10]
CsHsbNOH в среде смешанных растворителей диссоциированы меньше, чем в среде протолитических растворителей. Это приводит к тому, что в одних случаях смеси апротонных растворителей с протолитиче-скими растворителями имеют относительные шкалы кислотности больше, чем у протолитических растворителей, а в других случаях - меньше. Так, добавление апротонного растворителя к спиртам приводит к увеличению шкалы кислотности, а добавление его к кетонам и нитрилам, которые обладают большими шкалами, приводит к их уменьшению. [11]
Добавление апротонных растворителей, константа автопрото-лиза которых теоретически стремится к нулю, к протолитическим приводит к уменьшению A s смешанных растворителей. С другой стороны, апротонные растворители характеризуются низкими значениями диэлектрической проницаемости, поэтому НСЮ4 и ( C2H5) 4N OH в среде смешанных растворителей диссоциированы меньше, чем в среде протолитических растворителей. Это приводит к тому, что в одних случаях смеси апротонных растворителей с протолитическими растворителями имеют относительную шкалу кислотности больше, чем у протолитических растворителей, а в других случаях - меньше. Так, добавление апротонного растворителя к спиртам, имеющим небольшие шкалы кислотности, приводит к увеличению, а добавление к кетонам и нитрилам, которые обладают большими шкалами кислотности, приводит к уменьшению относительной шкалы кислотности. [12]
Добавление апротонных растворителей, константа автопрото-лиза которых теоретически стремится к нулю, к протолитическим приводит к уменьшению Ks смешанных растворителей. С другой стороны, апротонные растворители характеризуются низкими значениями диэлектрической проницаемости, поэтому НСЮ4 и ( СгНбЬ ОН в среде смешанных растворителей диссоциированы меньше, чем в среде протолитических растворителей. Это приводит к тому, что в одних случаях смеси апротонных растворителей с протолитическими растворителями имеют относительную шкалу кислотности больше, чем у протолитических растворителей, а в других случаях - меньше. Так, добавление апротонного растворителя к спиртам, имеющим небольшие шкалы кислотности, приводит к увеличению, а добавление к кетонам и нитрилам, которые обладают большими шкалами кислотности, приводит к уменьшению относительной шкалы кислотности. [13]
Добавление апротонных растворителей к другим растворителям приводит к изменению Es смешанных растворителей. Апротонные растворители имеют малую диэлектрическую проницаемость, поэтому НС1О4 и ( C2H5) sNOH в среде смешанных растворителей диссоциированы меньше, чем в среде протолитических растворителей. Это приводит к тому, что в одних случаях смеси апротонных растворителей с протолитическими растворителями имеют относительные шкалы кислотности больше, чем у протолитических растворителей, а в других случаях - меньше. Так, добавление апротонного растворителя к спиртам приводит к увеличению шкалы кислотности, а добавление его к кетонам и нитрилам, которые обладают большими шкалами, приводит к их уменьшению. [14]
Страницы: 1