Добавление - индифферентный электролит
Cтраница 1
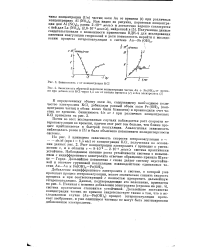 |
Зависимость v от концентрации КС1.| Зависимость обратной величины концентрации частиц Аи Fe ( OH3 от времени при добавлении КС1 через 1 5 час от начала процесса ( 1 и без электролита ( 2. [1] |
Добавление индифферентного электролита к системе, в которой уже протекает процесс гетерокоагуляции, может значительно снизить скорость процесса и при соответствующей с полностью прекратить дальнейшую гетерокоагуляцию. Начиная с момента добавления электролита ( стрелка на рис. 4), система практически становится устойчивой. Дальнейшее постоянство концентрации частиц во времени свидетельствует также о том, что в исследованном случае ( Аи-Fe ( OH) 3) процесс гетерокоагуляции протекает необратимо, и уже слипшиеся частицы не могут быть пептизированы добавленным электролитом. [2]
Добавление индифферентного электролита или присутствие нескольких растворенных солей ( например, в случае окислительно-восстановительных потенциалов) очень сильно уменьшает омическую поляризацию, так что она больше не имеет существенного значения. В присутствии только одного бинарного электролита удельное сопротивление раствора электролита вблизи поверхности электрода при достижении предельной плотности тока становится чрезвычайно большим. [3]
Однако добавление индифферентного электролита или присутствие несколько растворенных солей сильно уменьшает омическую составляющую. [4]
Таким образом, добавление индифферентных электролитов обычно приводит к уменьшению адсорбируемости органических веществ, особенно при потенциалах, удаленных от фн. [5]
Например, значительное уменьшение значений коэффициентов диффузии при добавлении индифферентного электролита в случае низкой концентрации ( 0 01 М) фона обусловлено главным образом влиянием межионных сил. Ионы С1 - соединяются с центральным атомом, поэтому за счет понижения заряда частицы и, следовательно, уменьшения ее гидратации уменьшается также объем диффундирующей частицы. Однако в случае образования иона РЬСЦ -, вероятно, происходит увеличение объема частицы, что приводит к уменьшению значения коэффициента диффузии. [6]
Например, значительное уменьшение значений коэффициентов диффузии при добавлении индифферентного электролита в случае низкой концентрации ( 0 01 / И) фона обусловлено главным образом влиянием межионных сил. Ионы С1 - соединяются с центральным атомом, поэтому за счет понижения заряда частицы и, следовательно, уменьшения ее гидратации уменьшается также объем диффундирующей частицы. [7]
Так как реакция протекает в области потенциалов ЕЕг, добавление индифферентного электролита, например хлорида натрия, приводит к увеличению скорости диссоциации. Как оказалось, в о М растворе индифферентного электролита эта скорость настолько велика, что на частотах, использованных Геришером при измерениях фарадеевского импеданса, равновесие, возможно, достигается. [8]
Поэтому в случае восстановления катиона предельный ток сильно уменьшается после добавления индифферентного электролита к исследуемому раствору. [9]
Миграционный ток, обусловленный переносом ионов под действием электростатических сил, устраняется добавлением индифферентного электролита. [10]
Составляющие ФАИ iR в полярографии сведены к минимуму из-за большой рабочей поверхности электрода сравнения и добавления индифферентного электролита ( фона), понижающего сопротивление раствора R. [11]
Из приведенных данных по исследованию устойчивости дисперсии алмаза в растворах КС1 следует, что в зависимости от рН дисперсионной среды и концентрации электролита и, как следствие этого, от состояния поверхности дисперсия алмаза ведет себя либо как лиофилизованная ( кислая область), либо как ионно-стабилизированная ( щелочная область) дисперсная система, обнаруживая тем самым различную чувствительность к добавлению индифферентного электролита. В зависимости от состояния поверхности частиц алмаза ( соотношения числа диссоциированных и недиссоциированных поверхностных групп), возможности образования водородных связей между молекулами воды и поверхностными группами алмаза, а также от концентрации добавленного электролита меняется структура воды в ГС, и, как следствие, соотношение между молекулярной, ионно-электростатической и структурной составляющими энергии взаимодействия частиц. [12]
В большинстве случаев работают при высокой ионной силе и относительно малых концентрациях комплексообразующих веществ, так что общую ионную концентрацию можно считать практически постоянной. Определенная ионная сила создается путем добавления индифферентного электролита ( нейтральной соли), не участвующего в комплексообразовании. [13]
Несмотря на то что оба материала характеризуются высоким перенапряжением кислорода, реакция Кольбе протекает только на платине при потенциале более высоком, чем потенциал выделения кис юрода Добавление индифферентных электролитов, конкурирующих с ацетат ионами при адсорбции на электроде, снижает выход продуктов реакции Кольбе. В среде метанола, где адсорбция выражена слабее, чем в воде, реакция Кочьбе протекает как на платиновом, так и на золотом анодах. [14]
Требование равенства ионной силы сливаемых растворов может быть выполнено почти всегда, когда имеют дело с открытием или определением малых количеств в объекте известного состава. Сюда относятся случаи установления чувствительности химических реакций, открытие примесей в реактивах, или, вообще говоря, анализ системы в основном известного состава на присутствие малых количеств какого-либо компонента. Здесь значение ионной силы можно точно или приближенно подсчитать и затем довести до желаемого добавлением индифферентного электролита, который почти всегда может быть выбран без особого труда. [15]
Страницы: 1 2