Добавление - посторонний электролит
Cтраница 1
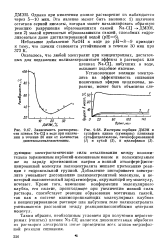 |
Зависимость растворимо - [ IMAGE ] Изотермы сорбции ДМЭМ и. [1] |
Добавление постороннего электролита уменьшает диссоциацию полиэлектролитной молекулы, и некоторый положительный заряд атмосферы, окружающей эту молекулу, исчезает. Кроме того, изменение конформации молекулярного клубка, его сжатие, происходящее при увеличении ионной силы раствора, способствует реакции образования мостичных связей, так как в системе взаимопроникающих молекулярных клубков в концентрированном растворе или набухшем геле полиэлектролита уменьшаются расстояния между реакционноспособными центрами молекул. [2]
Эффект уменьшения силы тока исчезает при добавлении постороннего электролита; концентрация электролита должна быть достаточно велика, если он содержит однозарядный катион, и очень незначительна для электролита с поливалентным катионом. [3]
Из уравнения Гендерсона следует, что при добавлении постороннего электролита величины и и v сближаются, в результате диффузионный потенциал резко уменьшается. [4]
Из уравнения Гендерсона следует, что при добавлении постороннего электролита величины а и и сближаются, в результате диффузионный потенциал резко уменьшается. [5]
Рэндал при изучении активностей в многокомпонентных системах установили, что в области разбавленных растворов при добавлении постороннего электролита изменение активности данного вещества определяется только концентрацией и валентным типом добавляемого вещества, но не его природой. [6]
Как видно из рис. 57, кривая зависимости адсорбции от рН для свежеприготовленных растворов проходит через два максимума. Добавление постороннего электролита понижает адсорбцию в области подъема кривой и подавляет второй максимум. [7]
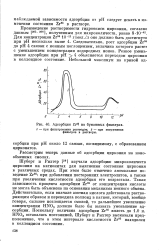 |
Адсорбция Zrs § на бумажных фильтрах. [8] |
При этом было отмечено аномальное поведение Zr95: при добавлении посторонних электролитов, а также при увеличении кислотности адсорбция его возрастала. Такая зависимость процента адсорбции Zr95 от концентрации кислоты не могла быть объяснена на основании механизма ионного обмена. Действительно, если вначале азотная кислота действовала растворяющим образом и переводила коллоид в катион, который, вообще говоря, сильнее поглощается смолой, то дальнейшее увеличение концентрации HN03 должно было бы вызвать уменьшение адсорбции. [9]
Практически при постепенном добавлении постороннего электролита величина предельного тока уменьшается сначала очень быстро, а затем медленно и, наконец, когда концентрация фона станет в 50 раз больше концентрации восстанавливающегося вещества, дальнейшее уменьшение силы тока при добавлении фона прекращается, что и указывает на полное устранение миграции. Поскольку все уравнения в полярографии выведены для чистых диффузионных токов, наличие миграционных токов нежелательно, и от них освобожу даются добавлением постороннего электролита. [10]
Скорость окислительно-восстановительных реакций очень сильно изменяется от присутствия посторонних веществ. Нормальные окислительно-восстановительные потенциалы, приведенные в приложении 5, относятся только к растворам, не содержащим посторонних ионов. Всякое добавление посторонних электролитов, изменяя ионную силу раствора, немедленно сказывается на величине окислительно-восстановительного потенциала. [11]
Скорость окислительно-восстановительных реакций очень сильно изменяется от присутствия посторонних веществ. Нормальные окислительно-восстановительные потенциалы, приведенные в Приложении 5, относятся только к растворам, не содержащим посторонних ионов. Всякое добавление посторонних электролитов, изменяя ионную силу раствора или рН среды, немедленно сказывается на величине окислительно-восстановительного потенциала. [12]
Страницы: 1