Дальнейшее добавление - титрант
Cтраница 1
 |
Взаимосвязь между i - Е - кривыми ( а и кривой потенцио-метрического титрования при постоянном токе с одним поляризуемым. [1] |
Дальнейшее добавление титранта не приводит к существенному изменению потенциала электрода. [2]
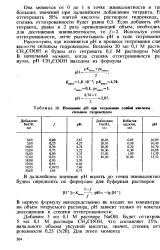 |
Изменение рН при титровании слабой кислоты сильным гидроксндом. [3] |
Она меняется от 0 до 1 в точке эквивалентности и та ] больших значений при дальнейшем добавлении титранта. [4]
При соответствующих условиях нерастворимый продукт реакции сохраняется в виде суспензии почти до самой точки эквивалентности; дальнейшее добавление титранта вызывает коагуляцию коллоида или растворение осадка, резкое уменьшение помутнения, что указывает на достижение конечной точки титрования. Таким образом, продукт реакции выполняет функцию индикатора. Примером такого рода может служить титрование анионных детергентов катионными и наоборот, а также титрование никотина кремневольфрамовой кислотой. [5]
Так как ионы Н обладают наиболее высокой подвижностью, то при добавлении ВОН вначале вследствие замены Н на менее подвижные ионы В электропроводность раствора падает. В точке эквивалентности х достигает минимальной величины, а по мере дальнейшего добавления титранта за счет появления гидроксил-ионов и катионов В снова возрастает. [6]
Протекание реакций окисления - восстановления, комнлексообразования и других сопровождается замет -, ным изменением магнитной восприимчивости. При постепенном добавлении титранта магнитная восприимчивость увеличивается или понижается до точки етехиометричности, после чего дальнейшее добавление титранта не вызывает изменений. [7]
Протекание реакций окисления - восстановления, ком плексообразования и других сопровождается заметным изменением магнитной восприимчивости. При постепенном добавлении титранта магнитная восприимчивость увеличивается или понижается до точки стехиометр-ичности, после чего дальнейшее добавление титранта не вызывает изменений. [8]
Степень оттитрованности показывает долю вещества, которая была оттитрована стандартным раствором в ходе титрования. Она меняется от 0 до 1 в точке эквивалентности и также больших значений при дальнейшем добавлении титранта. [9]
Графическим представлением хода титрования является кривая титрования. В общем смысле кривая титрования является функциональной зависимостью между логарифмом концентрации одного из реагентов и количеством, добавленного титранта или пропорциональной этому количеству степенью оттитрованы ости f, значения которой изменяются от 0 до 1 в эквивалентной точке и ббльших значений при дальнейшем добавлении титранта. В практическом смысле под понятием кривой титрования обычно подразумевается график зависимости измеренной величины ( функции концентрации) от объема добавленного титранта или степени оттитрованности. Если измеренная величина точно пропорциональна логарифму концентрации, чтс имеет место, например, при потенциометрическом титровании, то практическая кривая титрования идентична теоретической. В других случаях практическая кривая титрования, представляющая собой, например, график изменения поглощения излучения ( спектрофотометрическое титрование), электропроводности ( кондуктометрическое титрование) или силы тока ( амперометрическое титрование), отличается по форме от теоретической кривой титрования. [10]
В этом виде полярографии измеряется ток при определенном потенциале, находящемся в области плато предельного диффузионного тока определяемого вещества. Часто к этому методу относят титрование с амперо-метрическим определением конечной точки - амперо-метрическое титрование. Форма кривых амперометриче-ского титрования зависит от типа реакции титрования. Если титруемое вещество является электрохимически активным, а титрант нет, то ток с увеличением объема добавленного титранта уменьшается почти до нуля ( в точке эквивалентности) и затем остается постоянным при дальнейшем добавлении титранта. Если электрохимически активен титрант, а титруемое вещество нет, то ток остается близким к нулю до точки эквивалентности, после которой он начинает увеличиваться пропорционально концентрации добавляемого титранта. Если оба компонента реакции электрохимически активны, а продукты реакции нет, то получается V-образная кривая с минимумом, соответствующим точке эквивалентности. Метод титрования с индикатором применяется в тех случаях, когда ни определяемое вещество, ни титрант не дают в условиях определения полярографических волн или их получение по тем или иным причинам затруднительно. В этом случае к раствору титруемого вещества добавляется индикатор, дающий полярографическую волну и вступающий в реакцию с титрантом после того, как прореагирует определяемое вещество. В процессе титрования ток вначале ( до связывания всего титруемого вещества) будет оставаться постоянным, а затем он начинает уменьшаться до некоторой минимальной величины, и дальнейшее добавление титранта не будет влиять на ток. Кривая этого вида титрования имеет форму волны и перегиб на ней указывает на достижение точки эквивалентности. Эта точка определяется как середина перегиба кривой титрования. [11]
В этом виде полярографии измеряется ток при определенном потенциале, находящемся в области плато предельного диффузионного тока определяемого вещества. Часто к этому методу относят титрование с амперо-метрическим определением конечной точки - амперо-метрическое титрование. Форма кривых амперометриче-ского титрования зависит от типа реакции титрования. Если титруемое вещество является электрохимически активным, а титрант нет, то ток с увеличением объема добавленного титранта уменьшается почти до нуля ( в точке эквивалентности) и затем остается постоянным при дальнейшем добавлении титранта. Если электрохимически активен титрант, а титруемое вещество нет, то ток остается близким к нулю до точки эквивалентности, после которой он начинает увеличиваться пропорционально концентрации добавляемого титранта. Если оба компонента реакции электрохимически активны, а продукты реакции нет, то получается V-образная кривая с минимумом, соответствующим точке эквивалентности. Метод титрования с индикатором применяется в тех случаях, когда ни определяемое вещество, ни титрант не дают в условиях определения полярографических волн или их получение по тем или иным причинам затруднительно. В этом случае к раствору титруемого вещества добавляется индикатор, дающий полярографическую волну и вступающий в реакцию с титрантом после того, как прореагирует определяемое вещество. В процессе титрования ток вначале ( до связывания всего титруемого вещества) будет оставаться постоянным, а затем он начинает уменьшаться до некоторой минимальной величины, и дальнейшее добавление титранта не будет влиять на ток. Кривая этого вида титрования имеет форму волны и перегиб на ней указывает на достижение точки эквивалентности. Эта точка определяется как середина перегиба кривой титрования. [12]
Страницы: 1