Циклобутановое кольцо
Cтраница 2
Несмотря на ограниченность числа исследованных соединений, можно предполагать, что указанные линии характерны для углеводородов, содержащих циклобутановое кольцо. [16]
Заметим, что длины связей С-С в этих молекулах сильно отклоняются от стандартного значения 1 535 А, в частности связь между циклобутановыми кольцами имеет длину около 1 59 А. [17]
Напротив, втетрафенилцикло-бутане [66], фотодимере циклопентанона [67], 1 2 3 4-тетрациан-циклобутане [68], октаоксициклобутане [69], / праис-циклобутан-1 3-дикарбоновой кислоте [70] циклобутановое кольцо было найдено плоским. [18]
Чтобы объяснить такое различие, сначала заметим, что соединение А представляет собой циклобутановое кольцо с двумя 1 3 -этиленовыми мостиками, а соединение Б - циклобутановое кольцо с двумя бутадиеновыми мостиками. [19]
Примеры, изображенные на рис. 2 - 1 - 2 - 4, умышленно подобраны из числа молекул, имеющих два повторяющихся структурных элемента, а именно циклобутановое кольцо с двумя или четырьмя smop - бутильными группами. Сама по себе e / no / э-бутильная группа уже имеет асимметрический атом углерода. Тем не менее из четырех структур, показанных на рис. 2 - 1 - 2 - 4, только одна ( рис. 2 - 4) обладает оптической активностью. Молекула, изображенная слева на рис. 2 - 1, имеет плоскость симметрии, делящую цикл пополам, как показано на рисунке. Ее зеркальное изображение ( рис. 2 - 1, справа) можно совместить с исходной молекулой путем простого переноса влево. Молекула, показанная на рис. 2 - 2, обладает центром, или точкой, симметрии в центре кольца. В молекуле, изображенной на рис. 2 - 3, имеется зеркально-поворотная ось симметрии четвертого порядка, проходящая через центр цикла под прямым углом к нему. Ее нельзя сов-местить с зеркальным изображением ( рис. 2 - 4, справа), так что обе молекулы, изображенные на рис. 2 - 4, являются оптически активными. [20]
Исходным продуктом для синтеза красителей этого типа является тетрафторэтилен, который вводят в реакцию циклоприсоединения с акрилонитрилом или его винильными производными Полученный нитрил ( 1 2), содержащий циклобутановое кольцо, гидролизом нитриль-ной группы превращают в карбоновую кислоту ( 13), а затем переводят кислоту в ее хлоранг. [21]
Уже начиная с середины 40 - х годов стали появляться данные, указывающие сначала на аномально высокую длину связей С-С в производных циклобутана, а затем и на то, что в некоторых его производных циклобутановое кольцо, по-видимому, не копланар-но. Относительно копланарности кольца можно было заключить, что оно либо согнуто по диагонали под углом примерно 20, либо обладает большой амплитудой колебаний атомов, выходящих из плоскости кольца. [22]
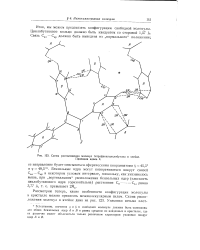 |
Схема расположения молекул тетрафенилциклобутана в ячейке. [23] |
Циклобутановое кольцо должно быть квадратом со стороной 1 57 А. [24]
Рассмотрение моделей показывает, что в циклобутане имеется два типа ориентации, до некоторой степени аналогичных аксиальным и экваториальным положениям в циклогексане. Если в циклобутановом кольце имеется два неполярных заместителя в положениях 1 и 3 относительно друг друга, ттгракс-изомер имеет экваториально-аксиальную конформацию, а г ис-изомер может быть либо диэкваториальным, либо диаксиальным. Простые расчеты ван-дерваальсовых взаимодействий ( разд. [25]
ТГФ более эффективен, чем натрий в толуоле. Спирт ( 4) имеет относительно напряженное циклобутановое кольцо, но окислением СгОй в пиридине и восстановлением по Вольфу - Кижнеру его легко превратить в желаемый углеводород. [26]
Четыре из них ( LXXVIII а - г) могут рассматриваться как структуры, в которых два бензольных кольца связаны в орго-положениях. Структура LXXVIII г может бытьпред-ставлена как содержащая циклобутановое кольцо с четырьмя экзоциклическими двойными связями. Наконец, структура LXXVIII д может рассматриваться, как подлинное производное циклобутадиена. [27]
На его основе получена большая группа фоторезистов негативного типа. Фотохимическое превращение этих резистов заключается в образовании мостиковых циклобутановых колец за счет этиленовых групп, принадлежащих разным полимерным цепям. [28]
Четыре из них ( LXXVIII a - г) могут рассматриваться как структуры, в которых два бензольных кольца связаны в орто-положениях. Структура LXXVIII г может быть представлена как содержащая циклобутановое кольцо с четырьмя экзоциклическими двойными связями. Наконец, структура LXXVIII д может рассматриваться, как подлинное производное циклобутаднена. [29]
На основании приведенного выше механизма можно предсказать, что метка 18О ( если используется Н 8О2) будет находиться в карбонильном кислороде амида. Предполагая, что углы связей в 1 2-дици-анэтилене составляют 120, а циклобутановое кольцо является плоским и заместители кольца образуют между собой углы 0 или 109 5, можно рассчитать ди-польные моменты следующих соединений: чис-1 2-дицианэтилен, ц2 - 4 000830 6 9 Д; транс - 1 2-дицианэтилен, f 0 Д; г ис-1 2-дицианциклобутан, ц8Д; транс - 1 2-дицианциклобутан. [30]
Страницы: 1 2 3