Этилениминное кольцо
Cтраница 1
Этилениминное кольцо в продукте реакции сохраняется. [1]
Конденсированное этилениминное кольцо, по-видимому, обязательно для биологической активности. Эта структура устойчива к щелочам и сохраняет активность при всех обусловленных действием щелочей структурных изменениях. Этилениминная группа крайне чувствительна к кислото-катализируемому сольво-лизу, и ее разрушение приводит к утрате биологической активности. [2]
В основу разработанной нами методики по изучению степени размыкания этилениминных колец взят метод количественного определения этилениминных групп, разработанный В. Г. Немецом, основанный на взаимодействии производных этиленимина с тиосульфатом натрия, согласно упомянутой схеме. [3]
Кроме того, было показано [44], что при наличии в этилениминном кольце свободной СН2 - группировки замещенные этилен-иминн полимеризуются так же легко, как и этиленимин, тогда как в отсутствие таковой ( например, в транс-2 3-бутиленимине и 2 2-диметил - З - к-пропилэтиленимине) полимеризация чрезвычайно затруднена. [4]
Рядом авторов были изучены и предложены в качестве лечебных препаратов соединения с этилениминными кольцами. [5]
Таким образом, полученные данные указывают на определенную зависимость между токсичностью и скоростью размыкания этилениминных колец. [6]
Прямое кислотное титрование [1, 2, 24, 27-31] проводится в разбавленных водных растворах на холоду, во избежание нуклеофильного раскрытия этилениминного кольца анионом кислоты. Для определения конца титрования используются кислотно-основные индикаторы, такие как метиловый красный и метиловый оранжевый, или потенциометрическая методика. [7]
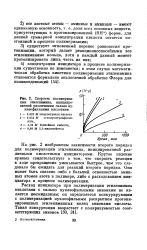 |
Скорость полимеризации этиленимина, инициированной различными сильно ну-клеофильными кислотами. [8] |
Расход инициатора при полимеризации этиленимина кислотами с сильно нуклеофильными анионами не является неожиданным; он определяется конкурирующим с полимеризацией нуклеофильным раскрытием протони-зированных этилениминных колец анионами кислоты. [9]
Этилениминные кольца 2 6-диэтиленимино - 4-хлорпиримидина ( самого токсичного из изученных) размыкаются быстрее всех, и в то же время размыкание этилениминных колец тетраэтиленимида п-фенилендифос-форной кислоты ( наименее токсичного) происходит наиболее медленно. [10]
Эти данные позволяют приписать 1: 2-соединению этиленимина с водой циклическую структуру хелатного гидрата, образованного путам межмолекулярного О - Н - и N - Н - связывания, менее компактную, однако, чем этилениминное кольцо. Так, две полосы поглощения в спектре этого соединения ( три 3580 - 3300 и 2200 - 2150 см-1) свидетельствуют в пользу Межмолекулярно связанных ОН - и NH-групп, а промежуточный ( между этилен-имином и зтаноламином) сдвиг частоты CN-растяжения интерпретируется как результат сохранения им циклической структуры. [11]
Изучение кинетики раскрытия протонизированных этилениминных циклов большим числом нуклеофилов, включавшим С1 - [387], Br -, J - [388], S2O32 - [387-389], НСО3 - [387], CNS - [388] и тиомочевину [388, 390] ( см. табл. 23), показало, что скорость рассматриваемых реакций определяется нуклеофильным характером аниона и в значительно меньшей степени зависит от замещения в этилениминном кольце. [12]
Следовательно, исключается возможность этилениминной структуры для этого соединения. Кроме того, известно, что этилениминное кольцо раскрывается под действием разб. [13]
В то время как реакционная способность хлорэтиламинов изучена довольно широко, вопрос устойчивости этилениминов освещен недостаточно. Поэтому мы решили изучить скорость размыкания этилениминных колец в некоторых полученных нами производных этиленимина. [14]
Раствор морцида в кукурузном масле, хранившийся в холодильнике, оставался стабильным в течение столь же долгого периода. Следует отметить, что эти данные основаны на определении неизмененного этилениминного кольца и, таким образом, возможно, не отражают фактического содержания неизмененного морцида. [15]
Страницы: 1 2