Комбинация - орбиталь
Cтраница 1
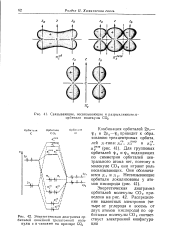 |
Связывающие, несвязывающие и разрыхляющие я-орбитали молекулы СО2.| Энергетическая диаграмма ор-биталей линейной трехатомной молекулы с л-связями на примере СО. [1] |
Комбинация орбиталей 2pz - 1р3 и 2ру - т з5 приводит к обра, зованию трехцентровых орбита. [2]
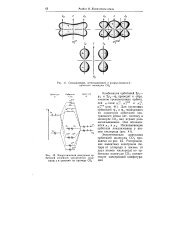 |
Связывающие, несвязывающие и разрыхляющие я-орбитали молекулы СО2. [3] |
Комбинация орбиталей 2pz - г) 3 и 2 / 7у - о) 5 приводит к обра, зованию трехцентровых орбита. [4]
Комбинация орбиталей типа одной -, трех р-тл одной d - приводит к sp3 rf - гибридизации. [5]
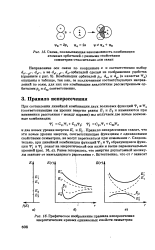 |
Схема, показывающая невозможность комбинации.| Графическое изображение правила непересечения энергетических кривых одинаковых свойств симметрии. [6] |
Комбинации орбиталей рг, dxz и dy2 ( в качестве Ч д) опущены в таблице, так как, за исключением соответствующих направлений по осям, для них все комбинации аналогичны рассмотренным ор-биталямру и dxy соответственно. [7]
 |
Схема образования связывающей и разрыхляющей молекулярных яг-орбиталей.| Нулевое перекрывание орбиталей. [8] |
При комбинации орбиталей р-типа характер перекрывания 2рх - ор-биталей существенно отличается от перекрывания 2ру - и 2р2 - ор-биталей. [9]
Вклады в комбинации орбиталей двух двойных связей от обеих молекул теперь не одинаковы: метильная группа. [10]
Какие из комбинаций орбиталей атомов водорода и фтора энергетически наиболее приемлемы для образования молекулярных орбиталей. [11]
Какие из комбинаций орбиталей атомов водорода и фтора приводят к образованию связывающей, разрыхляющей и несвязывающих орбиталей, если за ось, соединяющую атомы в молекуле HF, принять ось к. [12]
Следовательно, такая комбинация орбиталей к акту химического взаимодействия дае приводит. [13]
Установим, какие комбинации орбиталей можно построить из 2s - и 2 / 7-орбиталей атома азота. [14]
 |
Возмущение вырожденных уровней.| Относительные уровни энергии а -, я - и несвязывающих орбиталей к их взаимодействие с а - и я - уровнями. [15] |
Страницы: 1 2 3 4