Комплекс - железо
Cтраница 2
 |
Реакция. A1Y - Fe3 7 - FeY - Als. [16] |
Комплекс железа ( HI) с ЭДТА значительно устойчивее комплекса алюминия с ЭДТА, и поэтому указанное равновесие сдвигается вправо. [17]
 |
Реакция. A1Y - Fe3 7 - FeY. [18] |
Комплекс железа ( III) с ЗДТА значительно устойчивее комплекса алюминия с ЭДТА, и поэтому указанное равновесие сдвигается вправо. [19]
Комплексы железа в котловых водах парогенераторов разных давлений при комплексной обработке различны по составу и количеству. [20]
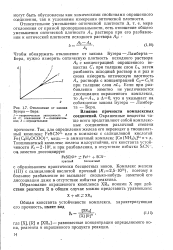 |
Отклонение от закона та - Бера. [21] |
Комплекс железа ( III) с салициловой кислотой прочный ( / Ci 2 5 - 1016), поэтому и большое разбавление не вызывает сколько-нибудь заметной его диссоциации даже в отсутствие избытка реактива. [22]
Хлорндные комплексы железа ( II), например FeCl2, поглощают и в видимой области спектра, но светопоглощение в УФ-об-ласти значительно выше. [23]
Галогено-я-аллилтрикарбонильные комплексы железа реагируют с трифенилфосфином, при этом происходит замещение одной СО-группы. Соединение с хлором было слишком не устойчиво, и его не удалось выделить, но соединения с бромом и иодом дают стабильные производные монотрифенилфосфина, окрашенные от темно-красного до коричневого цвета. [24]
Тепгракарбонилъные комплексы железа с этиленом [83] и бутадиеном [84] общей формулы Fe ( CO) 4 ( олефин) были получены прямой реакцией Fe2 ( GO) 9 с олефиновыми соединениями. В данном случае лиганд, вероятно, связан с металлом двойной углерод-углеродной связью. Первоначально такое предположение высказали на основании результатов ИК-спектроскопичес-кого исследования Кеттль и Оргел [85] для производного акрилонитрила. Фактически молекула Fe ( CO) 4 ( CH2CHCN) представляет собой тригональную бипирамиду [ ср. Fe ( CO) 5l, в которой одно из экваториальных положений занято центральной углерод-углеродной двойной связью. Расстояние между атомом железа и обоими винильными углеродными атомами составляет 2 09 и 2 10 А. [25]
Фенилизонитрильный комплекс железа Fe ( GO) 4GNPh получен также при взаимодействии карбонила железа с фенилизотиоцианатом. [26]
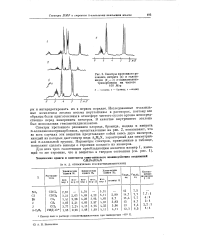 |
Спектры протонного резонанса нитрата ( а и галоге-нидов ( б - г л-аллилжелезо-трикарбонила на частоте. [27] |
Исследованные я-аллиль-ные комплексы железа весьма неустойчивы в растворах, поэтому все образцы были приготовлены в атмосфере чистого сухого аргона непосредственно перед измерением спектров. В качестве внутреннего эталона был использован гексаметилдисилоксан. [28]
Салицилатные и гидроксаматные комплексы железа окрашены в красно-коричневый цвет, комплекс с оксинафтойной кислотой ( с молярным соотношением 1: 1) - в синий цвет, а комплексы с тироном - в зеленый ( с молярным соотношением 1: 1), фиолетовый ( 1: 2) и светло-желтый ( 1: 3) цвета. В противоположность металлохромным индикаторам важным отличительным признаком всех перечисленных индикаторов является слабая окраска их комплексов ( молярные коэффициенты экстинкции около 103); поэтому, чтобы наблюдать эту окраску, необходимо применять индикаторы в концентрации, приблизительно в 10 раз превышающей концентрацию титруемого железа. Титрование проводят только в кислой среде ( рН 1 - 4), так как при рН 4 эффективные константы устойчивости комплексов металла с индикатором и с ЭДТА мало отличаются одна от другой. [29]
Страницы: 1 2 3 4 5