Комплекс - магний
Cтраница 2
 |
Типичная подпрограмма солохром фиолетового R S в присутствии магния ( рН 11, пиперидиновый буфер. [16] |
В присутствии магния волна эриохром черного Т уменьшается вследствие образбвания комплекса магния с реагентом. Снижение высоты волны пропорционально концентрации магния. Определению магния не мешает 20-кратный избыток Са, 10-кратный избыток Fe, A1 и Cd. Мешают Си, Zn, Mn и Со в равных количествах. [17]
Например, осуществив экстракционное отделение метилизобутил-кетоном при рН 10 5 комплекса магния с 8-оксихи НОЛином, магний в экстракте можно определить различными способами. Аналитическое окончание может быть фотометрическим, пламенно-фотометрическим и атомно-абсорбционным. Отметим, что пламенно-фотометрическое окончание позволяет определять магний с чувствительностью, на порядок превосходящей чувствительность фотометрического окончания. Однако в ряде случаев, особенно при определении элементов, обладающих хромофорным действием, более эффективным является именно фотометрическое окончание. [18]
При рН 9 индикатор имеет окраску от розовой до оранжевой, комплекс магния при рН 9 5 - 10 5 синего цвета. [19]
Диоксан и этанол меньше влияют на чувствительность метода и на устойчивость комплекса магния. При увеличении рН от 9 5 до 10 5 оптическая плотность медленно возрастает, а при рН 10 5 быстро падает. [20]
При рН 10 max составляет для реагента 640 нм, для комплекса магния 580 - 600 нм. В эквивалентной точке окраска раствора меняется от красной до синей. Можно титровать магний на холоду, но эквивалентная точка более четкая при - 60 С; добавление нескольких миллилитров ацетона или этанола делает изменение окраски в эквивалентной точке более резким. [21]
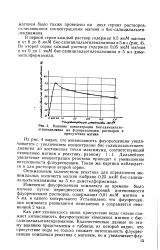 |
Влияние концентрации бис-салицилаль. [22] |
Как уже указывалось выше, присутствие воды сильно снижает интенсивность флуоресценции комплекса магния с бис - салицилальэтилендиамином. [23]
В описанных выше условиях хроматографирования большинство металлопорфиринов не подвергается деметаллированию, исключение составляют лишь комплексы магния. Поскольку даже следовые количества кислоты могут привести к деметаллированию, магнийсодержащие комплексы следует хроматографиро-вать в присутствии оснований и полностью исключить хлороформ из состава систем растворителей. [24]
Титрование надо проводить при такой длине волны, которой соответствует наибольшая разница в поглощении индикатора и комплекса магния. По мнению некоторых авторов [ 1293а ], при малых количествах магния эквивалентную точку более точно можно установить при 660 нм, при этой длине волны получается более крутой изгиб на кривой титрования. [25]
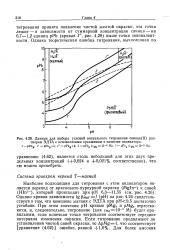 |
Данные для выбора условий визуального титрования свинца ( II рас. [26] |
Однако кривая зависимости lg pMgv / ( pH) на рис. 4.24 свидетельствуете о том, что комплекс магния с ЭДТА при рН9 5 достаточно устовдшв. При этом значении рН кривые pMg & и pMge пересекаются, и, следовательно, титрование ( для см8 10 - 2 М) будет правильным, если конечная точка титрования соответствует середине интервала изменения окраски. [27]
 |
Зависимость между скоростью ферментативной реакции и концентрацией субстрата ( о или фермента ( 6. [28] |
Пауш и Маргерум [22] применяли дифференциальные кинетические методы с остановкой струи в реакциях между ионами РЬ и комплексами магния, кальция, стронция и бария с транс - 1 2-ди-аминциклогексан - N, N, N, N - тетраацетатом ( 1 2 - ЦГДТА), в результате которых образуется комплекс свинца с 1 2 - ЦГДТА. Отношение констант скорости реакций выражается числами 1; 6 5; 96 и 1660 соответственно для магния, кальция, стронция и бария. [29]
В настоящее время изучено значительное число комплексов аналогичного состава, из которых наибольший интерес с практической точки зрения представляют собой комплексы магния, алюминия и бора. [30]
Страницы: 1 2 3 4