Комплекс - молибден
Cтраница 2
По данным Шелдона [44], комплексы молибдена эфирной природы типа Mo02 ( OR) 2 могут быть получены нагреванием Мо02 ( асас) 2 с гликолями. Именно таким образом получены комплексы с пропиленгликолем, 1 2-октандиолом, 2 3-диметилбутан - 2 3-ди-олом, а также цис - и игранс-1 2-циклогександиолами. [16]
Если к желто-оранжевому водному раствору пирокате-хинатного комплекса молибдена прибавить пиридин, никакого заметного изменения окраски не происходит. Однако если эту смесь встряхивать с хлороформом, последний окрашивается в красно-фиолетовый цвет. Очевидно, образуется пирокатехинатно-пиридиновый комплекс молибдена, не способный существовать в водном растворе. Для развития окраски максимальной интенсивности необходим довольно большой избыток пиридина по отношению к пирокатехину. Однократной экстракцией не удается перевести весь молибден в новый комплекс. [17]
Метод основан на измерении светопоглощения рода-нидного комплекса молибдена на фотоэлектроколори-метре при А эф 508 нм. [18]
Метод основан на измерении светопоглощения рода-нидного комплекса молибдена при Я 470 нм. Определению не мешают тантал и цирконий. Ниобий маскируют лимонной кислотой. [19]
 |
ДСТС спектра. [20] |
Исследования показали, что в оксогалогенидных комплексах молибдена и хрома первым замещается внеплоскостной лиганд, а затем - лиганды в плоскости. Такие исследования возможны во всех случаях, когда лиганд содержит ядра, дающие при взаимодействии с неспаренным электроном ДСТС. [21]
Полагают, что это соединение представляет собой карбонильный тетрафенилциклобутадиеновый комплекс молибдена. С W ( CO) 6 происходит аналогичная реакция. [22]
Данная глава посвящена некоторым общим свойствам комплексов молибдена с серусодержащими и флавиновыми лигандами, и ее можно рассматривать как введение в проблему моделирования некоторых конкретных молибденовых ферментов. [23]
Условия, необходимые для количественного образования комплексов молибдена и вольфрама, были предметом значительных исследований, и полученные данные свидетельствуют о существовании некоторых противоречий. Однако ясно, что комплекс молибдена образуется в кислой области рН, и что при этом не требуется восстановителей. В отношении вольфрама высказаны два совершенно различных предложения: согласно одному из них реакция проводится в горячей сильно кислой среде в присутствии восстановителя, согласно другому - реакция дол-лена идти в горячем слабокислом растворе без добавления восстановителя. [24]
Аналогичная ситуация возникает и при взаимодействии оксотетрафтор-ацетонитрильного комплекса молибдена с этиловым спиртом. Этоксогруп-па замещает не ацетонитрильную группу, расположенную против атома кислорода, а один из атомов фтора. При последующем замещении вторая этоксогрупиа занимает место молекулы ацетонитрила, а не второго атома F, поскольку образование еще одной четверной л-донорной связи невозможно, а замещение по транс-координате происходит легче. [25]
 |
Две проекции структуры Cu ( OH IO3. a - вид сверху. б - вид сбоку, причем октаэдричсскпе цепочки перпендикулярны плоскости чертежа. [26] |
Однако в то время как в комплексе молибдена расстояния металл - металл даже короче, чем в металлическом молибдене, в комплексе урана расстояния U-U ( 3 85 А) такие же большие, как в UOs, из чего можно заключить, что комплекс удерживается связями U-О. Из молекул такого же типа построены и гидроксид-оксиды цинка и свинца МбО4 ( ОН) 4 ( разд. [27]
Возможно, что при-этом активными частицами являются комплексы молибдена ( VI) и ванадия ( V), которые легко образуются в условиях реакции. [28]
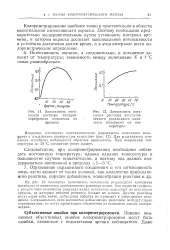 |
Зависимость погашения раствора толидин-серебряного комплекса от времени.| Зависимость погашения раствора восстановленного роданидного комплекса вольфрама от температуры. [29] |
На рис. 13 приведена зависимость погашения рсданидиэго комплекса молибдена от количества прибавленного роданида калия. Как видно из графика, с увеличением количества роданида калия погашение возрастает до некоторого предела, за которым избыток реактива больше не влияет. Другие реактивы могут вести себя иначе, добавление избытка их приводит к уменьшению погашения. Следовательно, если количества добавляемых реактивов не будут строго нормироваться, то могут происходить отклонения от основного закона колориметрии. [30]
Страницы: 1 2 3 4