Комплекс - фаза
Cтраница 1
Комплекс фаз, находящихся в равновесии для двойных систем, довольно разнообразен. Так, нонвариантные системы получаются для следующих комплексов фаз: 1) четыре твердые фазы; 2) три твердые и жидкая фаза; 3) две твердые, жидкая и газовая фазы и 4) три твердые и газовая фазы. [1]
Каждому комплексу фаз, находящихся в данной системе в равновесии, соответствует на диаграмме состав - свойство ( диаграмма состояний) определенный геометрический образ. [2]
Фазы ( Л ВДЖ) и комплексы фаз ( Ж Л, Ж В, Ж S, B S, 5 Л) указаны на соответствующих полях. [4]
Область, отвечающая отдельной фазе или комплексу фаз, называется пространством состояния. Правило о соприкасающихся пространствах состояния заключается в том, что два разных пространства состояния, разделенные друг от друга линией ( называемой пограничной), различаются между собой на одну фазу. Например, поле Ж и поле Ж - f В, разделенные линией В Е, отличаются на одну фазу. [5]
Согласно принципу соответствия в состоянии равновесия каждому комплексу фаз в системе соответствует определенный геометрический образ на диаграмме состав-свойство. Иногда этот принцип интерпретируется так: число кривых, из которых состоит диаграмма ликвидуса, равно числу твердых фаз, кристаллизующихся из жидкости [ 1, стр. [6]
Согласно второму принципу, каждой фазе ( или комплексу фаз) системы отвечает определенный геометрический образ на химической диаграмме. В дополнение к данному принципу Н. С. Курнаковым в 1912 г. было введено понятие о сингулярных ( дальтоновских) точках химической диаграммы. Сингулярной называется точка на химической диаграмме, отвечающая определенному недиссоциированному химическому соединению. Какое бы физическое свойство ни изучалось для данной системы ( температура плавления, вязкость, плотность и др.), эта характерная точка диаграммы ( точка максимума, точка минимума или точка пересечения двух ветвей одной и той же кривой) всегда леж т при одном и том же химическом составе. [7]
Принцип соответствия может быть сформулирован следующим образом: каждому комплексу фаз, находящихся в данной системе в равновесии, соответствует на диаграмме определенный геометрический образ. [8]
Принцип соответствия может быть сформулирован следующим образом: каждому комплексу фаз, находящихся в данной системе в равновесии, соответствует на диаграмме определенный геометрический образ. [9]
Принцип соответствия указывает, что каждой фазе или каждому комплексу фаз системы отвечает определенное геометрическое построение на химической диаграмме. Иными словами, изображение должно соответствовать изображаемому. [10]
Принцип соответствия устанавливает, что каждому физико-химическому индивидууму или каждому комплексу фаз, находящихся в данной системе в равновесии, отвечает определенный геометрический образ на химической диаграмме. [11]
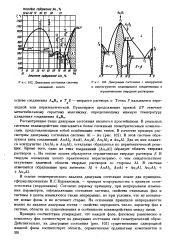 |
Диаграмма состояния системы алюминий - золото.| Диаграмма состояния с конгруэнтно. [12] |
Принцип соответствия утверждает, что каждой фазе, фазовому равновесию и комплексу фаз соответствует на диаграмме состояния свой геометрический образ. [13]
Первый из них - принцип соответствия - формулируется следующим образом: каждой фазе или каждому комплексу фаз, находящихся в равновесии, соответствует определенный элемент диаграммы. Мы имели возможность многократно проиллюстрировать применение этого принципа к разнообразным диаграммам. [14]
Известно, что азотирование стали ведет к образованию па ее поверхности азотированного слоя, состоящего из комплекса фаз системы железо-азот. Па скорость формирования азотированного слоя и на концентрацию азота в нем, что особенно важно для антикоррозионного азотирования, существенно влияют следующие технологические факторы: температура, время выдержки, степень диссоциации аммиака, равномерность и скорость подачи аммиака к поверхности обрабатываемых изделий. [15]
Страницы: 1 2 3
