Комплекс - фенол
Cтраница 1
Комплексы фенолов с гексаметилентетрамином разделяются эфирами или другими кислородными соединениями. Фенолы переходят в экстрагент, тогда как гексаметилентетрамин ( твердый или в растворе) не экстрагируется. [1]
Сходные результаты были получены также для комплексов фенолов с аминами. Выяснение типа связи в комплексах фенолов эффективно проводится по УФ-спектрам поглощения. Известно, что полоса ХЬЬ, соответствующая я-я - переходу в молекулах фенолов, испытывает красный сдвиг как при образовании комплексов с водородной связью, так и при ионизации с образованием фенолят-иона. В последнем случае, однако, сдвиг примерно на порядок больше. В частности, в [55-57] было установлено существование равновесия ( 3) в растворах, содержащих га-нитрофенол и третичные амины в ряде растворителей. [2]
В литературе приводятся данные о некоторых комплексах фенола с указанными веществами. [3]
Недостатками выбранного метода анализа являются длительность развития окраски комплекса фенола с пирамидоном и неустойчивость окраски во времени. [4]
Интересно также, что полоса ассоциированных групп ОН комплексов фенола с карбонильными соединениями, по-видимому, асимметрична, в то время как соответствующая полоса для комплексов фенола с эфирами симметрична. Этот вопрос был рассмотрен Дункеном и Фриче [87] и Фриче [90, 91], которые предположили две формы комплекса, одна из которых более стабильна при повышенных температурах и не зависит от концентрации акцептора протонов. Хейнен [88] уточнил это представление, предположив существование двух несколько различных поворотных изомеров комплекса фенол - ацетон. Это одно из возможных объяснений, но при попытках установить наличие или отсутствие таких изомеров следует иметь в виду, что асимметричные полосы легко получаются также в смешанных растворителях, таких, как смесь четы-реххлористый углерод - хлороформ. [5]
Этильный радикал сильнее действует на сдвиг электронов кислорода, чем бутильный, поэтому константа Кз комплекса фенола с этилацетатом будет выше, чем у комплекса с н-бутилацетатом. Согласно уравнению ( IV-9), с повышением константы Кз увеличивается коэффициент распределения фенола для этилацетата по сравнению с н-бутилацетатом. [6]
Исследование проводилось следующим образом: фенол предварительно насыщался фтористым бором до постоянного веса, после чего комплекс фенола с ВРз загружался в круглодонную колбу, куда прибавлялась азотная кислота при температуре от Б Ь 20 при постоянной перемешивании. [7]
Исследование проводилось следующим образом: фенол предварительно Насыщался фтористым бором до постоянного веса, пойле чего комплекс фенола с BFs загружался в круглодонную Йолбу куда прибавлялась азотная кислота при температуре от 5 ib 20 при постоянной перемешивании. [8]
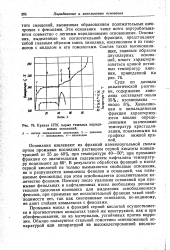 |
Кривая НТК сырых тяжелых пиридиновых оснований. [9] |
В результате обработки фракций и масел серной кислотой не только вымываются свободные основания, но и разрушаются комплексы фенолов и оснований, так называемые феноксйды; при этом освобождается дополнительное количество фенолов. Поэтому после удаления оснований при промывке фенольных и нафталиновых масел необходима дополнительная щелочная промывка для выделения освободившихся фенолов, при промывке же поглотительной фракции такой необходимости нет, так как хинолиновые основания, по-видимому, не дают стойких комплексов с фенолами. [10]
В качестве примера на рис. 1.17 показаны графики корреляции между lgA t и ДрА а для некоторых комплексов фенолов с пиридином и триэтиламином. Уравнение (1.3) было использовано Ратайчаком и Собчиком [329] для модификации соотношения, предложенного авторами данного обзора в 1964 г. [204], в котором в первом приближении коэффициент был принят равным единице. [11]
Заместители, вводимые в молекулу бензола или фенола, вступающих в комплексное соединение, оказывают такое же действие, что и при образовании комплексов фенолов с другими экстраген-тами. [12]
Интересно также, что полоса ассоциированных групп ОН комплексов фенола с карбонильными соединениями, по-видимому, асимметрична, в то время как соответствующая полоса для комплексов фенола с эфирами симметрична. Этот вопрос был рассмотрен Дункеном и Фриче [87] и Фриче [90, 91], которые предположили две формы комплекса, одна из которых более стабильна при повышенных температурах и не зависит от концентрации акцептора протонов. Хейнен [88] уточнил это представление, предположив существование двух несколько различных поворотных изомеров комплекса фенол - ацетон. Это одно из возможных объяснений, но при попытках установить наличие или отсутствие таких изомеров следует иметь в виду, что асимметричные полосы легко получаются также в смешанных растворителях, таких, как смесь четы-реххлористый углерод - хлороформ. [13]
Это, казалось бы, позволяет считать, что причина, обусловливающая протекание аци-лирования фенолов и, в частности, низкотемпературной полиотерификации, заключается не в образовании комплексов фенолов с хлорангидридами кислот. Однако чтобы четко ответить отрицательно или положительно на это предположение, необходимо более широкое исследование различных пар хлорангидридов и фенолов, так как пе исключена возможность, что в зависимости от их химического строения будет изменяться их способность к комплексообразованию. [14]
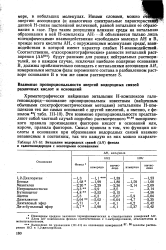 |
Энтальпии водородных связей ( АЯ фенола и галогеноводородов с некоторыми основаниями. [15] |
Страницы: 1 2