Комплекс - переходный элемент
Cтраница 2
Взаимодействие центральных ионов и лигандов может быть объяснено с помощью обобщенной теории кислот и оснований Льюиса, однако координационную связь можно рассматривать в принципе и как крвалентную с примесью ионной составляющей и описать ее методом ЛКАО. В комплексах переходных элементов важную роль играют d - орбитали, состояние которых зависит от пространственного расположения и типа лигандов. Для понимания электронного строения комплексов существенны данные об их электронных спектрах и магнитных свойствах, правильная интерпретация которых невозможна без рассмотрения характера расщепления d - орбиталей в полях различной симметрии. [16]
Качественно это наблюдение хорошо объясняется тем, что в результате снятия вырождения cf - орбиталей возникает подходящая энергетическая щель. Поскольку именно для комплексов переходных элементов типично неполное заселение d - орбиталей электронами, причина их окраски становится понятной; в отличие от этого в Са2 d - орбитали совсем не заняты электронами, в то время как в Zn2 они заселены полностью. [17]
Качественно это наблюдение хорошо объясняется тем, что в результате снятия вырождения d - орбиталей возникает подходящая энергетическая щель. Поскольку именно для комплексов переходных элементов типично неполное заселение d - орбиталей электронами, причина их окраски становится понятной; в отличие от этого в Са2 d - орбитали совсем не заняты электронами, в то время как в Zn2 они заселены полностью. [18]
В первой указаны соединения, содержащие серу, селен и теллур, во второй - комплексы с мостиками из атомов фосфора, мышьяка, сурьмы и висмута. В каждой части таблицы комплексы переходных элементов перечислены в следующем порядке: ванадий, хром, молибден, вольфрам, марганец, рений, железо, кобальт, никель, палладий и платина. [19]
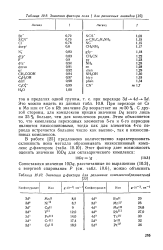 |
Значения фактора поля f для различных лигандов.| Значения g - фактора для различных комплексообразователей. [20] |
Этим объясняется то, что комплексы переходных элементов 5-го и 6-го периодов являются низкоспиновыми, тогда как для элементов 4-го периода встречается большое число как высоко -, так и низкоспиновых комплексов. [21]
Выше, в главе I, была дана общая характеристика комплексных соединений. Здесь мы рассмотрим кратко образование и свойства химических связей в комплексах переходных элементов ( см. также раздел III.7), ограничиваясь комплексами с координационными числами 4 и 6, так как именно такие числа характерны для подавляющего большинства известных в настоящее время комплексов. [22]
Зто правило отбора не является вполне строгим при наличии спин-орбитального взаимодействия. Поэтому иногда полосы запрещенных по спину переходов появляются в спектрах некоторых комплексов переходных элементов, но они, как правило, на один или два порядка слабее, чем полосы разрешенных по спину переходов. Их интенсивность увеличивается с увеличением константы спин-орбитального взаимодействия. [23]
Под термином комплекс подразумевается в этой главе обозначение тех соединений, которые содержат переходный и лантанидный ( или актинидный) металл с незаполненной соответственно d - или / - оболочками. Хотя мы рассмотрим и спектры комплексов лантанидов, основное внимание будет уделено комплексам переходных элементов первого переходного периода. Причина этого заключается в том, что, хотя спектры соединений элементов с конфигурациями 4сГ и 5dn и могут быть интерпретированы, их несколько труднее обсуждать с тех общих точек зрения, которые, по изложенным ниже соображениям, будут развиты в этой главе. Соединения с полностью заполненными оболочками не рассмотрены только из-за недостатка места; в действительности к ним применимы те же принципы. [24]
Работы по изучению строения комплексов с селеноцианато-группами, ближайшими аналогами тиоцианатогрупп, до недавнего времени практически отсутствовали. Это объясняется, по-видимому, сравнительной неустойчивостью селеноцианат-ных групп, препятствующей, например, получению селено-цианатных комплексов переходных элементов при проведении реакции в водных растворах. Однако за последние годы как в Советском Союзе, так и за рубежом были разработаны новые методы синтеза комплексных селеноцианатов и получено довольно много соединений этого класса. [25]
Гибридизация не ограничивается s - и р-орбиталями, но может вообще включать наложение всех типов атомных орбиталей. Гибриды, включающие d - орбитали, наблюдаются довольно часто у более тяжелых элементов и особенно важны в комплексах переходных элементов. [26]
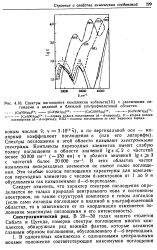 |
Спектры поглощения комплексов кобальта ( III с различными ли-гандамн в видимой и ближней ультрафиолетовой областях. [27] |
Спектры поглощения в этой области называют электронными спектрами. В этих областях частот комплексы непереходных элементов не имеют полос поглощения. Эти слабые полосы поглощения характерны для комплексов переходных элементов с числом d - электронов от 1 до 9 и обусловлены так называемыми d - d - переходами. [28]
Спектральная область, в которой находятся соответствующие полосы, лежит в ближней ИК -, видимой и УФ-областях спектра. Именно эти переходы в первую очередь ответственны за окраску комплексов переходных элементов. Практически эта область простирается от 10 000 до 30 000 см 1 ( 1000: - 333 нм), хотя некоторые d - d - переходы лежат и вне этого интервала. Наблюдение последних очень затруднительно, так как малые частоты часто экспериментально не доступны, а при более высоких частотах, вплоть до 50 000 см 1 ( 200 нм), эти полосы перекрываются более интенсивными полосами переноса заряда и интралигандными полосами. [29]
Изменение параметров а2 и у2 при замене стеклообразователя ( табл. 1) свидетельствует о возрастании степени ковалентности связи переходный металл-кислород в направлении Р206 - - Si02 - - В203, отражая возрастание степени ионности связи стекло-образующий катион-кислород в том же направлении. Зависимость параметров связей от природы модификатора является более слабой, чем от природы стеклообразователя, но, как следует из табл. 2, замена модификаторов в пределах одной группы периодической системы сопровождается хотя и слабым, но монотонным изменением параметров а2 в зависимости от положения элемента в группе. Переход от одной группы модификаторов к другой сопровождается большим изменением а2, которое, однако, нельзя вязать с положением модификатора в ряду периодической системы и которое обусловлено, по-видимому, различным расположением модификаторов различных групп относительно комплекса переходного элемента. [30]
Страницы: 1 2 3