Комплекс - галлий
Cтраница 2
Спектрофотометрически был определен состав комплексов галлия с пропил -, трихлорметил - и салицилфлуороном ( реагенты I, III и V), образующихся в кислой среде. В первом методе измерения выполнялись на спектрофотометре СФ-10 относительно воды после установления равновесия, которое наступало через 4 часа. С реагентами I и V были получены аналогичные результаты. [16]
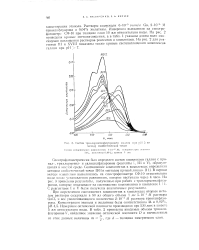 |
Состав трихлорметилфлуороната галлия при pil 5 по. [17] |
Спектрофотометрически был определен состав комплексов галлия с пропил -, трихлорметил - и салицилфлуороном ( реагенты I, III и V), образующихся в кислой среде. В первом методе измерения выполнялись на спектрофотометре СФ-10 относительно воды поелс установления равновесия, которое наступало через 4 часа. С реагентами I и V были получены аналогичные результаты. [18]
Аналогичные результаты получены [7] для комплекса галлия с пирокатехиновым фиолетовым. Комплексообразующим катионом является двухзарядный Ga ( OH) 2, реактив взаимодействует с галлием как ортооксихинон. [19]
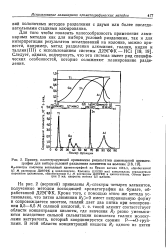 |
Пример, иллюстрирующий применение результатов ламинарной хроматографии для выбора условий разделения элементов на ( колонке. [20] |
Rf резко уменьшаются вследствие сильной сольватации комплекса галлия молекулами экстрагента, который координируется своими Р - нО - груп-пами. [21]
В технологии почти исключительно применяется экстракция хло-ридных комплексов галлия. Поэтому если требуется отделить железо, то его предварительно восстанавливают. [22]
Определение галлия основано на измерении интенсивности флуоресценции комплекса галлия с люмогаллионом в бифталатном буферном растворе при рН 2 2 - 2 7 [1,2] без отделения больших количеств кадмия. Мешают определению железо в количестве, большем 1 мкг, и медь в количестве, большем 5 мкг, при содержании от 0 05 до 0 5 мкг Ga з 10 мл раствора. [23]
Определение галлия основано на измерении интенсивности флуоресценции комплекса галлия с люмогаллионом без отделения больших количеств кадмия. Определению мешают более 1 мкг железа и 5 мкг меди. [24]
На основании литературных данных по константам устойчивости комплексов галлия и индия с морином и данных о состоянии этих элементов в растворе с учетом экспериментальных данных была сделана попытка рассчитать изменение концентрации металл-мориновых комплексов в процессе титрования этих элементов комплексоном. [25]
Определение галлия основано на измерении интенсивности флуоресценции комплекса галлия с люмогаллиоиом в бифталатном буферном растворе при рН 2 2 - 2 7 [1,2] без отделения больших количеств кадмия. Мешают определению железо в количестве, большем 1 мкг, и медь в количестве, большем 5 мкг, при содержании от 0 05 до 0 5 мкг Ga з 10 мл раствора. [26]
Комплексонометрическое определение основано на практически мгновенном образовании незначительно диссоциированного комплекса галлия с титрованным раствором комплексона. [27]
Из этой же таблицы, на примере флуоресценции комплексов галлия в водной среде и изоамиловом спирте, видно, что для люминесцентных реакций так же, как и для колориметрических, подтверждается положение относительно повышения чувствительности реакции при замене водной среды органическим растворителем. Это происходит потому, что в среде органического растворителя, имеющего меньшую диэлектрическую постоянную, уменьшается диссоциация комплексных соединений. В водной среде, кроме того, могут образовываться аквакомплексы, способствующие безызлучательным переходам возбужденной молекулы. [28]
Та н н и н о в ы и комплекс галлия подобен соответствующему комплексу алюминия. [29]
При высоком содержании в растворе алюминия, цинка и меди экстрагирование комплекса галлия затруднено. Большие количества меди и ванадия ослабляют интенсивность свечения органической фазы. [30]
Страницы: 1 2 3 4