Электронейтральный комплекс
Cтраница 1
Электронейтральные комплексы, следовательно, являются комплексными соединениями без внешней сферы. [1]
Из электронейтральных комплексов представлены только некоторые карбонилы металлов. [2]
Для электронейтральных комплексов применяются русские названия комплексообразователей в именительном падеже. [3]
Из электронейтральных комплексов представлены только некоторые карбонилы металлов. [4]
Когда образуется электронейтральный комплекс, он должен быть по возможности менее полярным. Например, если две метилыные группы в молекуле диацетилдиоксйма заместить фенильными группами, то получается бензилдио / ксим, / который образует еще более нерастворимый хелат с никелем ( II), чем хелат исходного реагента. [5]
Нетрудно видеть, что смешанные электронейтральные комплексы устойчивы лишь при температуре 180 С. [6]
Поэтому вполне вероятна диффузия электронейтральных комплексов Na - OJ в направлении мест, более благоприятных для стабилизации этих комплексов. Более вероятно, что при образовании значительно большего числа ( - 1020 спин / г) ионов С2 в NaY, содержащем ионизованные атомы Na, основной вклад в общий спектр Ог будут давать комплексы Na - Oj, локализованные в обычных местах каркаса. [7]
Согласно высказанному предположению о циклическом строении электронейтральных комплексов, увеличение электроотрицательности заместителей у одного атома фосфора в молекуле диокиси и уменьшение электроотрицательности заместителей у другого атома фосфора может привести к усилению взаимодействия с NaJ в комплексной молекуле. Действительно, комплекс NaJ с несимметричной диокисыо ( и - СНзОСвН4) 2Р ( 0) - СН2 - P ( 0) ( C6H4GFS) 2 более устойчив, чем с соответствующими симметричными диокисями. [8]
Поскольку с увеличением прочности связано понижение рН образования электронейтральных комплексов, которые не поглощаются катиони-том, мы предположили, что глюконовая кислота должна быть хорошим элюентом для разделения РЗЭ на катионите. [9]
При этом образуется временный наведенный диполь; иногда - при растворении электронейтральных комплексов в некоторых неполярных инертных растворителях - это взаимодействие накладывается на дисперсионные взаимодействия. [10]
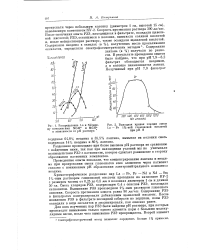 |
Выходная кривая элюции смеси. [11] |
Проведенные опыты показали, что концентрирование лантана и неодима при пропускании смеси гл: юконатов этих элементов через катионит связано с понижением рН образования электронейтрального комплекса неодима. [12]
Если металл экстрагируется из водного раствора в органический неполярный растворитель, то ион металла переносится через границу раздела жидкость-жидкость в виде незаряженной частицы, которая может представлять собой либо электронейтральный комплекс ( или хелат), образованный с органическим реагентом, либо ионно-асооциатный комплекс. [13]
Таким образом, на поверхности твердой фазы формируется двойной электрический слой, внутреннюю обкладку которого составляют потенциал-определяющие ионы, а внешнюю - противоионы. В целом электронейтральный комплекс называется мицеллой. [14]
Поведение ионных пар типа [ R4As Cl - ], где R - органический радикал, например фенильная группа, аналогично поведению комплексов металлов, рассмотренных выше, так как они электронейтральны и растворимы в органических растворителях. Однако природа сил, обусловливающих образование ионных пар и электронейтральных комплексов металлов, различна. В количественно экстрагируемом комплексе атомы лиганда занимают первую ( внутреннюю) координационную сферу иона металла и образуют с ним прочную связь. Каждый ион в ионной паре окружен молекулами растворителя, и эти ионы с их сольватными оболочками удерживаются вместе силами электростатического притяжения. В воде такие ионные пары неустойчивы и имеют очень короткие времена жизни. Однако если концентрация одной из частиц, образующих ионную пару, достаточно высока, то равновесная концентрация ионных пар будет достаточна для экстракции их в неполярную фазу, в которой они гораздо более устойчивы, как мы увидим из следующего примера. [15]
Страницы: 1 2