Белковый комплекс
Cтраница 2
Для хлебопекарных качеств зерна большое значение имеет его белковый комплекс ( клейковина), от которого зависит термоустойчивость зерна. При нагревании зерна происходит денатурация белков, причем степень денатурации зависит от температуры и влажности зерна. Следует отметить отсутствие единства мнений в показателях термоустойчивости зерна, так как разные исследователи применяли различные методы определения термоустойчивости. [16]
Однако большинство ценных компонентов клетки находится в виде различных белковых комплексов, поэтому добавление к среде на-тивных дрожжей не дает эффекта. [17]
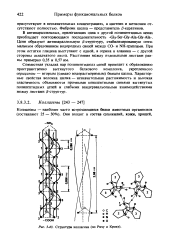 |
Структура коллагена ( по Ричу и Крику. [18] |
Совместная укладка пар полипептидных цепей приводит к образованию пространственно вытянутого белкового комплекса, укрепленного серицином - вторым ( однако водорастворимым) белком шелка. Характерные свойства волокна шелка - незначительная растяжимость и высокая эластичность объясняются прочными ковалентными связями вытянутых полипептидных цепей и слабыми вандерваальсовыми взаимодействиями между листами / 3-структур. [19]
Колоночную хроматографию применяют для разделения экстрагированных из растений природных белковых комплексов хлорофиллов или протохлорофиллидов. [20]
Гемосидерин в отличие от ферритина и трансферрина является водонерастворимым железосодержащим белковым комплексом, состоящим, кроме того, на 25 % из нуклеотидов и углеводов. Он содержится главным образом в ретикулоэндотелиоцитах печени и селезенки. Биологическая роль гемосидерина изучена недостаточно. [21]
Итак, транспорт витамина А в организме осуществляется преимущественно специфическим белковым комплексом, состоящим из ретинолсвязывающего белка и тироксинсвязывающего преальбумина. Секреция транспортных протеинов из печени регулируется при участии витамина А. Основным депо витамина А является печень, откуда ретинол поступает в кровь через пластинчатый комплекс для обеспечения метаболической потребности органов и тканей. Белковая недостаточность нарушает биосинтез в печени ретинолсвязывающего белка и тироксинсвязывающего преальбумина и приводит к снижению их уровня в крови. [22]
У некоторых микроорганизмов они входят в состав целлюлосомы - белкового комплекса, находящегося на клеточной поверхности. [24]
Как известно, уровень содержания сульфгидрильных групп отражает способность белковых комплексов крови связывать токсические вещества, циркулирующие в кревеноснои системе. Поэтому в наших исследованиях было предусмотрено изучение и этого показателя. [25]
Таким образом, транспорт витамина А в крови осуществляется сложным белковым комплексом, состоящим из ретинолсвязывающего белка - непосредственного носителя ретинола и тироксинсвязываюшего преальбумина, который, соединяясь с ретинолсвя-зывающим белком, предохраняет последний от клу-бочковой фильтрации и экскреции с мочой. Связывание витамина А с указанными протеинами имеет важное физиологическое значение в плане солюбилизации нерастворимого в воде ретинола, предохранения его от быстрого химического распада и элиминации с мочой, а также в плане доставки ретинола из депо в органы-мишени и передачи его в специфические рецепторные молекулы клеток, что необходимо для проявления специфических обменных функций витамина А в этих органах и тканях. Концентрация транспортирующих витамин А белков в плазме крови в нормальных условиях коррелирует с обеспеченностью организма витамином. Возможность подобной корреляции в определенной мере связана с тем, что витамин А является одним из регуляторов обмена собственных транспортных белков. [26]
Первый метод состоит в определении отдельных белковых групп в общем белковом комплексе. При этом отдельные белковые группы ( альбумины, глобулины, про-ламины, глютелины) извлекаются различными растворителями и количественно учитываются. Содержание белковых фракций в растениях различно. Даже в пределах одного и того же сорта качественный состав белков подвергается глубоким изменениям в зависимости от условий выращивания и других факторов. [27]
Для каждой масличной культуры установлены соответствующие влаго-тепловые режимы и оптимальная продолжительность воздействия на их белковый комплекс. [28]
 |
Ассоциация в растворах детергентов. [29] |
Благодаря высокой поверхностной активности и способности к растворению белков, липоидои, каротеноидов, диссоциации белковых комплексов, инактивации вирусов и бактериальных токсинов, гемолизу и мощному бактерицидному действию детергенты применяются для приготовления различных фармацевтических, дезинфицирующих, бактерицидных и фунгицидных препаратов. [30]
Страницы: 1 2 3 4
