Мономерный комплекс
Cтраница 2
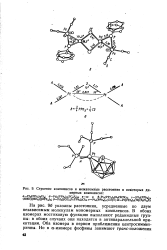 |
Строение комплексов и межатомные расстояния в некоторых ди. [16] |
На рис. 96 указаны расстояния, усредненные по двум независимым молекулам мономерных комплексов. В обоих изомерах мостиковую функцию выполняют роданидные группы: в обоих случаях они находятся в антипараллельной ориентации. Оба изомера в первом приближении центросиммет-ричны. [17]
Растворимость соединений этого типа в СС14 позволила определить частоты валентных колебаний NH в мономерных комплексах, исключив влияние межмолекулярных водородных связей, и измерить интенсивность соответствующих полос поглощения. Значения частот VNH и интенсивности используются Чаттом и др. в качестве мерила влияния, испытываемого амином со стороны лиганда L, находящегося по отношению к нему в т / анс-цоложении. [18]
Наличие в пара-положении электронодо-норных заместителей ( ОСН 3, СН 3) приводит к образованию мономерных комплексов, характеризующихся плохой термостойкостью. Когда заместителями служат акцепторы электронов ( С1, СООСН3), облегчается образование высокотермостойких димерных комплексов. На основании спектроскопических данных мономеру и димеру приписаны структуры 69а и 696 соответственно. [19]
Константы устойчивости образующихся при этом поликомплексов RMe имеют высокие значения, лишь незначительно уступающие соответствующим величинам мономерного комплекса MeL, где L - ОЭДТА ( см. табл. 52), и превышающие таковые для комплекса MeL, где L - иминодиуксусная кислота. [20]
С ( СН3) 3 аналогичный тетрамер Со ( асас) 2 тоже перестает существовать, но в этом случае образуются тетраэдрические мономерные комплексы кобальта. [21]
Гидриды трехвалентного бора в индивидуальном состоянии обычно представляют собой димеры, однако в эфирных растворителях, особенно в ТГФ, сам диборан существует в виде мономерного комплекса ВН3 - ТГФ. [22]
Гидриды трехвалентного бора в индивидуальном состоянии обычно представляют собой димеры, однако в эфирных растворителях, особенно, в ТГФ, сам диборан существует в виде мономерного комплекса ВН3 - ТГФ. [23]
Наиболее важный результат, полученный при исследовании этих реакций, состоит в том, что скорости реакций мостиковых комплексов приблизительно на два-три порядка выше скоростей для соответствующих мономерных комплексов. Это подтверждает наличие значительного напряжения в четырехчленных мостиковых системах, что приводит в результате к ослаблению связи Pt - X для мостиковой группы по сравнению с концевыми группами. [24]
Возможно также, что комплексы бериллия с м - и м - ОФИДА имеют димерное строение, что и сближает величины их констант устойчивости с константами устойчивости мономерных комплексов бериллия с о - ОФИДА. [25]
Примером может служить бензиллитий, который мономерен в тетрагидрофуране и реагирует в 104 раз быстрее, чем тетрамерный метиллитий с тем же субстратом. Упоминавшиеся выше мономерные комплексы с ТМЭДА также во много раз более активны, чем ассоциированные соединения. Литийалкилы могут давать полилитиевые производные с ацетиленами, ацетонит-рилом и другими соединениями. [26]
Иногда за счет образования полимерной сетки стабилизируются одноядерные структуры металлических комплексов, которые в отсутствие сетки образуют только двухъядерные структуры. В случае мономерных комплексов стабильны только двухъядерные структуры. Сшитый полистирол служит носителем Rh -, Ru - или Pd-комплексов, которые отличаются высокой каталитической активностью в процессах гидрирования. [27]
В контрольном препарате резко выделяется пик 530 ммк, соответствующий мономерному комплексу АО-ДНК. После гидролиза пик мономерного комплекса резко падает, но возникает пик в области 600 ммк. [28]
Как отмечалось выше, аналогичные реакции соединений платины приводят к стабильным мономерным комплексам. [29]
Константы / ск, / с, скорости нарастания вязкости, полученные из уравнений ( 1) и ( 2), отражают совокупность различных стадий процесса структурирования растворов комплексов, протекающих параллельно и последовательно. Формирование надмолекулярной структуры растворов комплексов при взаимодействии алкок-сидов бора и лития включает такие основные стадии, как образование мономерного комплекса, ассоциация его по литий-кислородной связи и алкильным фрагментам, ассоциация молекул растворителя иод влиянием комплекса. О связи происходят, очевидно, спонтанно и очень быстро. Суммарная скорость этих стадий зависит от концентрации исходных алкоксидов бора и лития. Лимитирующими стадиями скорости структурирования являются межмолекулярная ассоциация комплексов по алкильным заместителям, ориентация и упаковка молекул растворителя, которые приводят к повышению вязкости растворов. О связи, намного выше k скорости роста вязкости, которую в основном определяют более медленные стадии. Однако скорости медленных и быстрых стадий процесса структурообразования в растворах взаимозависимы. [30]
Страницы: 1 2 3