Фторидный комплекс - цирконий
Cтраница 1
Фторидный комплекс циркония не образует в указанных условиях малорастворимых соединений. [1]
Фторидные комплексы циркония характеризуются большой прочностью, вследствие чего открыть из них цирконий характерными реакциями не удается. [2]
Авторы объясняют это хорошей экстрагируемостью одного из фторидных комплексов циркония ( ZrF3) и плохой экстрагируемостью остальных. [3]
Раджан и Гупта [286] предлагают проводить вымывание фторидных комплексов циркония и гафния из анионообменных смол растворами серной кислоты. В этом случае первым вымывается гафний и достигается хороший разрыв между выходом циркония и гафния. Используя колонки размером слоя 6 5 х 120 см, заполненные смолами дауэкс-2 ( - 100 - - ( - 200 меш) и амберлит Щ А-400 ( - 85 Ч - - - - 200 меш), авторы получили спектрально чистые двуокиси циркония и гафния с выходом 91 - 94 и 75 % соответственно. [4]
К - Бабко [484] указывается, что константа нестойкости фторидного комплекса циркония имеет порядок 10 - 9 тогда как константы фторидных комплексов алюминия и железа 10 - 7 и lO 6, соответственно. Поэтому становится понятным, что добавление иона фтора вызывает обесцвечивание ализарин-цир-конового лака и других окрашенных соединений циркония с органическими реактивами. [5]
При взаимодействии с фторидом эти комплексы разрушаются в результате образования более прочного фторидного комплекса циркония. [6]
Окрашенный цирконализариновый комплекс ( лак) взаимодействует с фторидом с образованием более прочного фторидного комплекса циркония. [7]
В то же время степень образования комплекса для Zr ( IV) резко увеличивается с ростом концентрации H2SiF6, Зависимость констант образования фторидных комплексов циркония от концентрации HN03 имеет сложный вид, связанный, вероятно, с изменением ионного состояния циркония. [8]
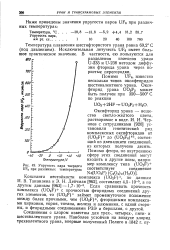 |
Упругость пара твердого UF6 при различных температурах. [9] |
Если сравнивать прочность комплекса ( UO2F) с прочностью фторидных соединений других элементов, то ( UO2F) займет промежуточное положение между более прочными, чем ( UO2F), фторидными комплексами циркония, тория, титана, железа и алюминия, с одной стороны, и фторидными соединениями РЗЭ и бериллия, с другой. [10]
 |
Колонка для распределительно-хроматографического экстрагирования. [11] |
Предложен [460] метод разделения циркония и алюминия при помощи анионита дауэкс-1. Метод основан на различной адсорбционной способности фторидных комплексов циркония и алюминия на этой смоле. Если пропускать через колонку со смолой дауэкс-1 раствор циркония и алюминия в 0 6 М НС1 и 0 8 М H2F2, то цирконий полностью адсорбируется на смоле, а алюминий переходит в фильтрат. [12]
В этом методе титриметрического анализа используются сте-хиометрически количественно и быстро протекающие реакции комплексообразования. В различных видах комплексиметрии применяют монодентатные лиганды - образование галогенидных комплексов ртути ( II) ( меркуриметрия), фторидных комплексов циркония ( фториметрия), и полидентатные лиганды - образование комплексов многими металлами с аминополикарбоновыми кислотами и их производными. [13]
Впоследствии метод выделения циркония был несколько видоизменен [61] и использован для определения циркония в силикатных породах и сплавах. Фторидный комплекс циркония очень прочен и хорошо поглощается анионптом в S04 - форме. В заключение цирконий элюируют 4М НС1 и определяют титрованием этилендиаминтетраацетатом. [14]
Известны методы определения фтора по обесцвечиванию железо-роданид-ного или циркоикй-ализаринатного комплексов. Колориметрическое определение основано на том, что фторид связывает ионы железа или циркония в малодиссоциированные фторидные комплексы, разрушая таким образом окрашенные соединения этих ионов. Максимально допустимая кислотность при образовании окрашенного комплекса зависит от относительной прочности фторидных комплексов железа и циркония. На основании описанного выше опыта можно сделать вывод, что использование более прочного фторидного комплекса циркония допускает применение значительно большей кислотности, чем при методах, основанных на образовании фторидных комплексов железа. [15]
Страницы: 1 2