Молекулярный комплекс
Cтраница 3
Образование молекулярных комплексов происходит в процессе конденсации. В этот момент, очевидно, создаются благоприятные для донорно-акцепторного взаимодействия ориентации молекул, а благодаря быстрому отводу тепла, выделяющегося при конденсации, эти нестойкие соединения успевают стабилизироваться. Молекулярные комплексы НВг-С3Н5С1 устойчивы лишь при весьма низких температурах. После нагревания замороженных смесей бромистого водорода с хлористым аллилом наблюдается изменение первоначального давления. По-видимому, образование конечных продуктов в стеклообразной смеси, содержащей молекулярные комплексы, происходит при достижении нижней границы интервала размягчения, что сопровождается сильным уменьшением вязкости. [31]
Образование молекулярного комплекса ослабляет связи во взаимодействующих молекулах и может способствовать образованию радикалов. Роль комплексов с переносом заряда в реакциях ацилирования рассмотрена в обзоре [472], в котором приведены результаты низкотемпературных исследований свойств комплексов, образующихся в твердофазных сублимированных смесях реагентов при 77 К, и отмечено, что при их нагревании происходят химические превращения. [32]
Изучение молекулярных комплексов, образуемых диполярными апротонными растворителями с протонодонорами за счет Н - связи. [33]
Область молекулярных комплексов настолько широка, что дать полный обзор ее в книге ограниченных размеров не представляется возможным. [34]
Образование равновесного молекулярного комплекса само по себе не влияет на скорость изотопного обмена водорода, поскольку, как мы видели выше, константа скорости реакции зависит только от начального ( мономерного) и переходного состояния. [35]
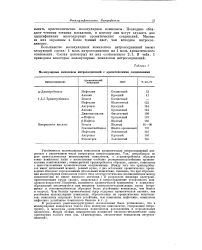 |
Молекулярные комплексы нитросоединений с ароматическими соединениями. [36] |
Большинство молекулярных комплексов нитросоединений имеют следующий состав: 1 моль нитросоединения на 1 моль ароматического компонента. В табл. 1 приведены некоторые молекулярные комплексы нитросоединений. [37]
Образование молекулярного комплекса состава 1: 1 позволяет объяснить и влияние на реакцию изменения состава смеси. Для смесей различного состава общий характер термографических кривых в своих основных чертах аналогичен кривым для состава, отвечающего стехиометрии комплекса. Однако с увеличением количества этилена в смеси реакция происходит при больших временах освещения. Это обусловлено тем, что кристаллы этилена разбавляют кристаллы молекулярного комплекса, что, естественно, затрудняет реакцию. [38]
Образование молекулярных комплексов хлороформа с ди-этиловым эфиром [2] и эфирами полиэтиленгликоля [3] были исследованы методом определения теплот смешения. [39]
Образование молекулярных комплексов воды, то есть процесс ассоциации, основан на соединении частиц Н О за счет водородных связей. [40]
Под молекулярным комплексом подразумевают ассоциат из двух или более молекул, в котором каждая молекула в значительной степени сохраняет свою химическую и физическую индивидуальность. [41]
В молекулярных комплексах наиболее важен октаэдриче-ский тип симметрии, изображенный на рис. 10.1. Приняв за направления осей х, у, z направления от центрального атома металла к лигандам, выберем такие же uf - орбитали, как в разделе 10.3. Основываясь на простой схеме, типа изображенной на рис. 10.2, можно сделать следующее заключение. Расщепление теперь будет таким, что орбитали dxy, dyz, d x останутся вырожденными и энергетически будут располагаться значительно ниже, чем орбитали dz, а у, которые тоже остаются вырожденными. Вследствие симметрии последние должны иметь те же особенности, что и dxi-yi. Отсюда следует, что любая их линейная комбинация - и в частности d - также должна вести себя аналогичным образом. [42]
Изоэлектронен ли молекулярный комплекс, состоящий из BF3 и NH3, какому-либо органическому соединению. [43]
Хингидрон ( молекулярный комплекс / г-бензохинона и гидрохинона) С6Н4С2 СбЩОНЬ; М 218 21; темно-з. [44]
Молекулы или молекулярные комплексы с ростом давления или температуры разрушаются и вещество переходит в чисто атомарное состояние. Электронные оболочки атомов перестраиваются, приобретая все более регулярное заполнение уровней. Одновременно происходит отрыв наружных электронов, определяющих химическую индивидуальность вещества. Наконец, если в процессе сжатия и нагревания вещество остается в твердом состоянии, то упорядочивается и его кристаллическая решетка. Проходя через серию структурных превращений, она становится все более плотно упакованной и приобретает в конечном счете единую для всех веществ объемно-центрированную кубическую структуру. [45]
Страницы: 1 2 3 4