Нейтрализованный комплекс
Cтраница 2
 |
Растворимость в системе NH3 - HNO3 - НаО. [16] |
Расчеты показывают, что масса испарившейся воды равна 15 61 кг, а нейтрализованного комплекса Ь - 84 39 кг. [17]
Графический анализ технологических показателей процесса получения аммофоса по обеим схемам позволяет определить состав нейтрализованных комплексов и соотношение жидкой и твердой фаз в этих комплексах на основных этапах процесса нейтрализации фосфорной кислоты аммиаком. Для первой схемы были определены составы нейтрализованных комплексов, поступающих во второй сатуратор и в аппарат АГ. [18]
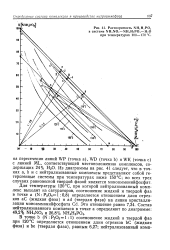 |
Растворимость МН4Н2РО4 в системе Н4МО3 - МН4Н2РО4 - Н2О при температурах 100 - 170 С. [19] |
Из диаграммы на рис. 41 следует, что в точках a, b и с нейтрализованные комплексы представляют собой гетерогенные системы при температурах ниже 150 С; во всех трех случаях равновесной твердой фазой является моноаммонийфосфат. [20]
В результате получим, что масса испарившейся воды равна 1069 1 кг, а оставшегося нейтрализованного комплекса состава точки с - 1476 9 кг. [21]
В точке f, где фосфорная кислота нейтрализована аммиаком до NH3: Н3РО41 39: 1, в нейтрализованном комплексе, содержащем 13 75 % NH3, 57 % Н3РО4 и 29 25 % Н2О, твердая фаза отсутствует. [22]
При выполнении графического расчета условно принимаем, что такое содержание влаги в комплексе достигается за счет испарения воды из нейтрализованного комплекса а. В этом случае отрезок линии испарения WD, соответствующий массе воды в оставшемся нейтрализованном комплексе, составляет 12 % всей длины линии WD, равной 330 лин. [23]
При увеличении степени нейтрализации фосфорной кислоты аммиаком до NH3: Н3РО42: 1, отношение Ж: Т в нейтрализованном комплексе ( точка w; 22 % NH3) 63 5 % Н3РО4 и 14 5 % Н2О) резко уменьшается, так как в этом комплексе кристаллизующийся диаммонийфосфат находится в равновесии с эвтоническим раствором EJ, состав которого соответствует наименьшей растворимости диаммонийфосфата. [24]
При анализе процесса нейтрализации азотной кислоты аммиаком в соответствии с первой технологической схемой 49 % - ную азотную кислоту нейтрализуют 100 % - ным аммиаком. Состав нейтрализованного комплекса на диаграмме изображается точкой а, лежащей на пересечении линии нейтрализации NB с линией WT. [25]
Их разряд хотя и требует лишь одного электрона, но вследствие прочности комплекса FeOH связан с большой энергией активации. Дальнейшие превращения нейтрализованного комплекса, включающие стадию присоединения еще одного электрона и приводящие к выделению металла на катоде, протекают без заметных торможений. [26]
Принимаем, что реакционная масса после выхода из выпарных аппаратов содержит 18 % воды. Точка q, характеризующая состав нейтрализованного комплекса, поступающего в аппарат БГС, расположена в области кристаллизации моноаммонийфосфата. [27]
Графический анализ технологических показателей процесса получения аммофоса по обеим схемам позволяет определить состав нейтрализованных комплексов и соотношение жидкой и твердой фаз в этих комплексах на основных этапах процесса нейтрализации фосфорной кислоты аммиаком. Для первой схемы были определены составы нейтрализованных комплексов, поступающих во второй сатуратор и в аппарат АГ. [28]
При выполнении графического расчета условно принимаем, что такое содержание влаги в комплексе достигается за счет испарения воды из нейтрализованного комплекса а. В этом случае отрезок линии испарения WD, соответствующий массе воды в оставшемся нейтрализованном комплексе, составляет 12 % всей длины линии WD, равной 330 лин. [29]
Составы нейтрализованного комплекса с наиболее распространенным соотношением: Р2О5 1.1 лежат на линии WD. Если концентрация исходной фосфорной кислоты 54 / р2о3, а азотной 47о / 0 HNQ3, то нейтрализованный комплекс по практическим данным содержит около 25 % Н2О Фигуративная точка комплекса лежит на пересечении линии WD с линией ML соответствующей положению комплексов, содержащих 25 % воды. [30]
Страницы: 1 2 3