Промежуточный поверхностный комплекс
Cтраница 1
Промежуточный поверхностный комплекс может разлагаться, так же как при реакции С - f Оз, под действием температуры и молекул водяного пара из газового объема. [1]
 |
& Независимость скорости ( и взаимодействия Н2О и С от давления Р паров воды при 2450 К. [2] |
Здесь, как и в реакции СО2 с С, имеет место образование промежуточных поверхностных комплексов, состоящих из атомов кислорода и поверхностных атомов углерода. В пользу этого говорит совпадение результатов ряда исследований в условиях вакуума в отношении порядка реакции ( нулевой), энергии активации ( 90 ккал) и отсутствия СС2 в продуктах реакции. [3]
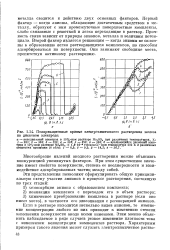 |
Поляризационные кривые электрохимического растворения железа на дисковом электроде. [4] |
Первый фактор - когда анионы, обладающие достаточным сродством к металлу, образуют с ним промежуточные поверхностные комплексы, слабо связанные с решеткой и легко переходящие в раствор. Прочность связи зависит от природы анионов, металла и величины потенциала. Второй фактор является решающим - когда анионы не склонны к образованию легко растворяющихся комплексов, но способны адсорбироваться на поверхности. Они занимают свободные места, препятствуя активному растворению. [5]
Вероятно, в большинстве случаев при адсорбции МОС происходит хе-ыосорбция с образованием того или иного типа промежуточного поверхностного комплекса МОС-подложка. Типы возможных комплексов рассмотрены раньше. Их устойчивость и преобладание того или иного типа комплекса определяется свойствами подложки и МОС, внешними условиями распада. [6]
Вторым этапом является образование промежуточного комплекса водяного пара с углеродом топлива. Промежуточный поверхностный комплекс получается с кислородом водяного пара. [7]
Если после окисления СО катализатор подвергнуть откачке, то стационарная концентрация комплекса С03 ( ад0) остается неизменной; но при глубоком обезгаживании этого катализатора, как и следует ожидать, происходит десорбция двуокиси углерода и кислорода. Особенность этого механизма состоит в том, что продукт реакции фактически может способствовать образованию промежуточного поверхностного комплекса. Однако имеются данные [18], свидетельствующие, что С02 не может десорбироваться спонтанно и что она тормозит скорость реакции. [8]
Детальный механизм реакций гидрирования СО может быть сформулирован исходя из общепризнанной сейчас точки зрения о глубокой химической сущности катализа при рассмотрении взаимодействия монооксида углерода и водорода с активными центрами катализатора. Основным фактором, определяющим динамику поверхностного механизма взаимодействия СО и Н2, вероятные маршруты превращений промежуточных поверхностных комплексов и, как следствие, направление реакции гидрирования монооксида углерода, является форма активации молекул СО и Н2, определяемая природой центрального атома металла, типом его лигандного окружения и внешними условиями синтеза, в первую очередь, температурой и давлением в системе. [9]
Общим недостатком при изучении кинетики окисления коксовых отложений на катализаторах является узкий интервал варьирования определяющих параметров: начальной степени закоксованности, концентрации кислорода и особенно температуры. Кинетические уравнения составлялись на основе гипотез о механизме, которые не учитывают даже хорошо установленные факты многостадийности окисления [3, 92], когда на первой стадии образуется промежуточный поверхностный комплекс углерода с кислородом. [10]
 |
Структура и атомные радиусы [ А ] металлов и некоторых неметаллов. [11] |
Здесь Ашмор вслед за Трепнелом, на которого он ссылается, делает существенную ошибку: мультиплетная теория А. А. Баландина с момента вэзникновения ( 1929 г.) не ограничивалась только принципом геометрического ( или структурного) соответствия, считая его одним из необходимых условий. Второй принцип теории, о котором ни Ашмор, ни Трепнел не упоминают - принцип энергетического соответствия - учитывает баланс энергий разрывающихся и образующихся при реакции связей, включая связи в промежуточных поверхностных комплексах. Оптимальным для катализа является структурное и энергетическое соответствия. [12]
С целью выяснения роли алкенов и водорода в процессе Cs-дегидроциклизации и изомеризации алканов исследованы [125] превращения 3-метилпентана, а также З - метилпентена-1, цис - и транс - изомеров 3-метилпен-тена - 2 на платиновой черни при температуре 300 - 390 С в токе Н2 и Не прицразличном содержании Н2 в газе-носителе. Выявлено четкое влияние концентрации Н2 в газе-носителе на превращения ( Cs-циклизация, скелетная изомеризация, образование метилциклопентана и бензола) 3-метилпентана и изомерных алкенов. Полагают [125], что скелетная изомеризация должна проходить через промежуточный поверхностный комплекс, общий для 3-метилпентана и 3-метилпентенов. Этому комплексу соответствует полугидрированное поверхностное состояние углеводорода, адсорбированного на двух центрах. При малом содержании Н2 возникает сильное взаимодействие между углеводородом и металлом с образованием кратных связей углерод-платина, что приводит к образованию З - метилпентена-1 из 3-метилпентана и. [13]
Причиной этих отклонений, очевидно, является невыполнение по крайней мере одного из постулатов, определяющих протекание процессов в идеальных адсорбированных слоях. Действительно, как следует из литературных данных, разные участки каталитических поверхностей одной и той же химической природы энергетически неравноценны, а прочность возникающих поверхностных соединений может быть различной. Это вызывается неодинаковой химической ненасыщенностью поверхностных атомов, захватом микропримесей, многообразием промежуточных поверхностных комплексов, разрывом поверхностных связей при адсорбции, смещением и образованием новых поверхностных фаз, изменением адсорбционной способности и каталитической активности при переходе от одних граней к другим. [14]
Имеются: некоторые доказательства того [30], что окислы металлов хемосорбируют насыщенные углеводороды в виде радикалов. Томас [52] наблюдал, что при адсорбции этана на стехиометрической закиси никеля зеленая вначале закись никеля становится серой. Такое изменение окраски может быть связано с модифицированием дефектной структуры твердого окисла. Поэтому представляется вероятным, что один из важных механизмов каталитического окисления насыщенных углеводородов заключается во взаимодействии адсорбированного кислорода с адсорбированными углеводородными радикалами с последующим расщеплением промежуточного поверхностного комплекса на более простые молекулы. Природа образующегося при этом конечного продукта, по-видимому, зависит от применяющегося окисла металла. [15]
Страницы: 1