Отрицательный комплекс
Cтраница 1
Отрицательный комплекс в названиях солей всегда получает окончание ат. [1]
На анионитах металлы сорбируются в виде отрицательных комплексов, и разрушение этих комплексов при введении комплексообразователя, образующего более устойчивые нейтральные или положительные комплексы с соответствующим металлом, или при изменении условий приводит к высоко специфичному выделению. Количество реагентов, способных образовывать в растворах комплексы со многими или отдельными элементами, весьма велико, и соответственно может быть предложено много различных вариантов группового и поэлементного разделений. [2]
На анионитах металлы сорбируются в виде отрицательных комплексов и разрушение этих комплексов при введении ком-плексообразующего реагента, дающего более устойчивые нейтральные или положительные комплексы с соответствующим металлом, или при изменении условий приводит к высоко специфичному выделению. Количество реагентов, способных образовывать в растворах комплексы со многими или отдельными элементами, весьма велико, и соответственно может быть предложено много различных вариантов групповых и поэлементных разделений. [3]
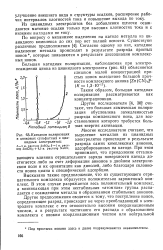 |
Катодная поляризация выделение металлов из цианидных в цинковых сульфатных и циа - электролитов происходит в результате. [4] |
Высказэно также предположение, что из существующего отрицательного комплекса образуется положительно заряженный комплекс. В этом случае разряжается весь положительный комплекс, а возникающая при этом нестабильная атомная группа распадается с осаждением металла и образованием стабильных анионов. [5]
 |
Адсорбция Aulne на угле. [6] |
Если Б области рН 0 Аи199 существует в виде хлораурат-ного отрицательного комплекса, то с ростом рН комплекс будет разрушаться и образовывать положительно заряженные продукты гидролиза. Одновременно увеличивается отрицательный заряд стекла. При рН 2, где заряд стекла еще более отрицателен, Аи199, очевидно, переходит в форму, заряженную одноименно со стеклом, что приводит к уменьшению адсорбции. В литературе приводится величина 8.5 - 10 46, следовательно, приведенное объяснение можно рассматривать как вероятное. [7]
 |
Максимумы полос поглощения кристаялофосфоров их водных растворов. [8] |
Существует и другая концепция [ 253 - 2571, согласно которой центры селективного поглощения и свечения представляют собой отрицательные комплексы типа ( MHaln) m -, образуемые ионами активирующей примеси с ионами решетки основания. [9]
Если вокруг положительного комплексообразователя координируются отрицательные лиганды, то положительный заряд комплексного иона понижается, а в пределе он переходит в отрицательный комплекс, например [ А1 ( ОН) 4 ] -, [ A1FJ3, Таким образом, получается комплексный анион, заряд которого равен алгебраической сумме окислительных чисел комплексообразователя и всех лигандов. [10]
 |
Псевдопотенциал, описывающий взаимодействие электрона и протона.| Псевдопотенциал, описывающий взаимодействие электрона и Cs-1 Обозначения те же, что и на 7. [11] |
Должно быть также па пм, ni п, пв п -, где геи, п, п - - концентрации молекул, положительных и отрицательных комплексов. [12]
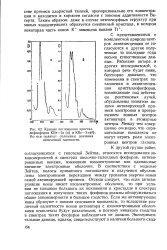 |
Кривые поглощения кристаллофосфоров КВг-In ( а и КВг-Sn ( 6. По оси ординат отложены значения оптической плотности. [13] |
Работами автора и других исследователей, о которых речь будет ниже, бесспорно доказано, что изменения в спектрах поглощения и люминесценции кристаллофосфоров, возникающие под действием рентгеновых лучей, обусловлены захватом ионами активирующей примеси электронов и превращением ионных центров активатора в атомарные центры. Между тем совершенно оч ( видно, что отрицательные комплексы не могут играть роли электронных центров захвата. [14]
Из особенностей вымывания с фторидных колонок следует, что, по-видимому, более вероятна сорбция отрицательно заряженных фторидных комплексов, чем осаждение на смоле нерастворимых фторидов. Поведение радия вызывает удивление, так как образование отрицательных комплексов кажется маловероятным, а RaF2 в заметной степени растворим. Было сделано предположение, что радий может соосаждаться с CaF2, который значительно менее растворим. [15]
Страницы: 1 2