Цианидный комплекс - золото
Cтраница 1
Цианидные комплексы золота известны давно. [1]
 |
Степень извлечения Е ( % германия из 60 раствора желатином в зависимости от диа - д метра d ( мм частиц сорбента. [2] |
В этой связи определенный интерес представляет изучение взаимного влияния цианидных комплексов золота и примесных соединений в процессе сорбции на анионитах. [3]
Для золочения металлов и сплавов используют также щелочные растворы, содержащие цианидный комплекс золота и гипофосфит натрия. Для осаждения золота на неметалл изделие опускают в ванну, содержащую хлорид золота, щелочь и восстановитель ( например, глюкозу или формальдегид-как в реакции серебряного зеркала), а затем высушивают. [4]
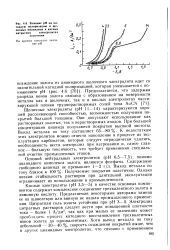 |
Влияние рН на катодную поляризацию в щелочных цианидных и кислых цнтратных электролитах. [5] |
Основой нейтральных электролитов ( рН 6 5 - 7 5), помимо цианидного комплекса золота, являются фосфаты. Однако низкая стабильность растворов при длительной эксплуатации ограничивает их использование в промышленности. [6]
Немалое значение имеют аниониты для извлечения и концентрирования золота из разбавленных растворов и из пульпы в виде цианидных комплексов золота, которые хорошо поглощаются на монофункциональных анионитах. Особенно интересно применение для этой цели анионита АН-18. [7]
В мерную колбу емкостью 50 мл помещают анализируемый раствор и к нему последовательно прибавляют 5 мл раствора тиомочевины ( для разрушения цианидного комплекса золота или серебра), 10 мл ацетатного буферного раствора и дистиллированную воду до объема 40 - 45 мл. Раствор термостатируют, прибавляют к нему 5 мл термостатированного раствора гекса-цианоферрата калия и доводят общий объем до 50 мл. Отсчет времени начинают с момента прибавления раствора гексациа-ноферрата калия. Одновременно проводят холостой опыт без соединения золота или серебра. Через 60 мин измеряют оптическую плотность раствора на фотоэлектроколориметре, используя светофильтр с ЭФФ. Вычитают из полученного значения оптической плотности ее значение для холостого опыта. [8]
Из реакции ( 125) следует, что растворение золота может происходить только при наличии в водном растворе кислорода, а конечным продуктом взаимодействия является анионный цианидный комплекс золота. Из многочисленных солей цианистоводородной кислоты для растворения золота наиболее пригодны соли щелочных и щелочноземельных металлов. В начале промышленного внедрения процесса цианирования использовали цианистый калий KCN, который позднее был полностью заменен более дешевым цианистым натрием NaCN. Он более дешев даже по сравнению с цианистым натрием, но его расход по сравнению с NaC N выше почти в два раза. [9]
На кафедре аналитической химии создана теория пластифицированных ИЧМ, которая позволяет выбрать и оптимизировать состав мембранной композиции для изготовления сенсоров для определения любых заряженных частиц; разработаны и исследованы ИСЭ для определения щелочных и щелочноземельных металлов, ацидокомплексов металлов, например анионных цианидных комплексов золота и серебра, ряда органических кислот и оснований. [10]
Второй случай сопряжения следовало бы считать наиболее вероятным, так как при совместном протекании электрохимических реакций на одной и той же поверхности следует ожидать тормозящего действия одной на другую - например, когда часть поверхности катализатора занята адсорбированными реагентами, промежуточными или побочными продуктами реакции. Такое торможение установлено в системе Ag - Ag ( CN) i - № Н4, где скорость катодной реакции осаждения серебра снижается ( на - 30 %) в присутствии гидразина, а цианидный комплекс серебра тормозит анодное окисление N2H4; аналогично действует цианидный комплекс золота на окисление борогидрида в системе Аи-Au ( CN) T - - ВЩ. [11]
Метод, разработанный А. Б. Даванковым и В. М. Лауфер [14, 15], основан на осаждении золота в слое ионита. В более поздних работах А. Б. Даванкова и В. М. Лауфер [16], а также И. Д. Фридман и Н. Н. Поповой [22, 23] используется поглощение цианидного комплекса золота анионитом. Анализируемый раст-вор ( 3 л), содержащий менее 2 - 10 - 5 % Аи в виде цианидного комплекса, встряхивают в течение 3 ч с 10 г анионита в С1 - форме. [12]
Страницы: 1