Полиметаллический комплекс
Cтраница 1
Полиметаллические комплексы, подобные бериллию, образует алюминий. В качестве примера на рис. 3 даны кривые титрования 1.10 - 3 М оксабисэтиленаминоизопропилфос-фоновой кислоты при одновременном присутствии 1.10 - 3 М алюминия и 1.1 Q-3 М ионов ( II) переходных элементов. [1]
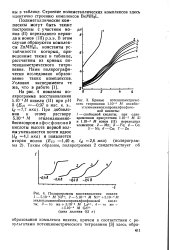 |
Кривые потенциометричес.| Подпрограммы восстановления никеля. / - - М № 2. 2 - - М Ni2 - 4 M этилендиаминобисизопропилфосфоновой кислоты. 3 -то же - 4 М La3. 4 - то же. [2] |
Полиметаллические комплексы могут быть также построены с участием ионов ( И) переходного периода и ионов ( 111) р.з.э. В этом случае образуются комплексы ZnMH2L, константы устойчивости которых, приведенные также в таблице, рассчитаны из кривых по-тенциометрического титрования. Нами полярографи-чески исследовано образование таких комплексов. [3]
Рассмотрены условия образования полиметаллических комплексов и выявлены области их существования в зависимости от степени протонизации лиганда. [4]
Рассмотрим несколько примеров образования полиметаллических комплексов. На рис. 1 даны кривые титрования 1.10 - 3 М этилендиаминобисизопропилфосфоновой кислоты при одновременном присутствии 1.10 - 3 М ионов ( II) металлов первого переходного периода и 1.10 - 3 М бериллия, а на рис. 2 то же, но в присутствии 2.10 - 3 М бериллия. [5]
Алюминий, подобно бериллию [2], образует полиметаллические комплексы с алкилендиаминобисалкилфосфоновы-ми кислотами с участием ионов ( II) переходных элементов Эти результаты будут рассмотрены в отдельной статье. [6]
В исследуемом нами случае ( гетерогенный катализ в присутствии координационных полиметаллических комплексов) молекулярный вес полимера обычно почти не зависит от времени полимеризации, если полимеризация продолжается более 10 мин. [7]
Методами рН - потенциометрического титрования и полярографии исследовано образование полиметаллических комплексов алкилендиаминобисалкилфосфоновых кислот. [8]
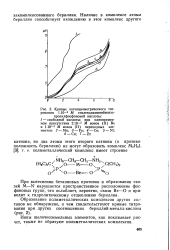 |
Кривые потенциометрического титрования - 3 М этилендиаминобисизо. [9] |
Ионы щелочноземельных элементов, как показывает расчет, также не образуют полиметаллических комплексов. [10]
В последние годы крайне интенсивно велись исследования в области металлических производных карбонилов металлов всех трех типов и особенно в области так называемых кластерных три - и полиметаллических комплексов, у которых переходные металлы связаны друг с другом в цикле представляющих интерес главным образом с точки зрения изучения природы их химической связи. [11]
Сопоставление молекул Fe3 ( CO) i2, Ru3 ( CO) i2 и Os3 ( COl2 кажется интересным не только с точки зрения тенденции тяжелых переходных металлов к образованию полиметаллических комплексов без участия мостиковых карбонильных групп, но и позволяет выявить еще одно отличие в свойствах металлов второго и третьего переходных рядов. Это отличие касается характера взаимодействия между атомами металлов. При сопоставлении длин связей Fe-Fe в молекуле Fe3 ( CO) i2 с удвоенным значением односвязного ковалентного радиуса атома железа 2 68 А можно видеть, что две из них длиной 2 68 и 2 69 А являются ординарными ковалентными, а третья длиной 2 55 А, как и полагается для связей металл - металл, укрепленных мостикойыми СОгруппами, сокращена на - 0 15 А по сравнению с удвоенным радиусом. [12]
Для остальных р.з.э. параметры этой волны имеют сходные значения. Таким образом, при образовании полиметаллического комплекса первая волна восстановления никеля ( II) сдвигается в отрицательную сторону, причем id ( NiLnH2L) id ( Ni), а вторая волна никеля ( II) вообще исчезает. [13]
Прочность комплексов ЭДУФ с катионом железа приблизительно равна прочности комплексов ЭДТУ, а комплексы ДТПУ не прочнее соответствующих комплексов ЭДТФ. Алюминий, так же как и бериллий, образует полиметаллические комплексы с алкилендиамин-бис-алкилфосфоновыми кислотами с участием ионов двухвалентных переходных элементов. [14]
Выпуск содержит две статьи. Вторая статья является обзором структур одноядерных карбонилсодер-жащих комплексов и, частично, строения полиметаллических комплексов. [15]
Страницы: 1 2