Биядерный комплекс
Cтраница 1
Биядерные комплексы [ СБН5М ( СО) 3 ] а ( М Сг, ОДо, W) получаются при кипячении М ( СО) в с избытком дициклопентадиена. Комплексы Мо и W могут быть получены также при пропускании паров циклопентадиена и гексакар-бонила металла сквозь трубку, нагретую до 280 - 350 С. Гексакарбонил хрома в этих условиях образует бисциклопентадиенилхром. [1]
Биядерные комплексы выделены Также в результате реакций, получивших название реакций окислительного присоединения. [2]
Все полученные закрепленные биядерные комплексы оказались каталитически активными в реакции гидрирования олефинов, причем было найдено, что в зависимости от структуры фрагмента Pdg изменяются их каталитические свойства в реакции гидрирования циклопентадиена в циклопентен и циклопентан. [3]
В биядерных комплексах реализуются связи со второй иминодиацетатной группировкой. Подобное явление может быть объяснено октаэдрической геометрией центральной координационной частицы Мо03 или МоО, ограничивающей число возможных связей с лигандами. [4]
В биядерном комплексе XLV ацетилен связан также лишь с одним атомом железа. [5]
Описаны также биядерные комплексы же-леза [ С5Н5ГеСО ] 2 ( СО) ( СК1: 1) с мостиковым ( R Ph) или терминальным ( R Me, f - Bu) изонитрилом. [6]
Методы синтеза биядерных комплексов и результаты их УФ, ИК, и РЭФ-спектроскопического исследования приведены в таблице. [7]
При образовании биядерных комплексов этих металлов наблюдается диссоциация обеих оксигрупп. Интересно отметить, что кривая титрования DL-ДОБТА в присутствии двукратного количества меди образует как бы две равные ступени, и двум последовательным стадиям комплексообразования соответствуют примерно равные константы устойчивости комплексов. Это свидетельствует о том, что в биядерных комплексах переходных металлов, вероятно, образуются две самостоятельные, практически равноценные симметричные координационные сферы с координацией депротонированных гидр-оксилов. Наиболее ярко проявляется участие оксигрупп, сопровождающееся диссоциацией гидрокислов, при координации железа. [8]
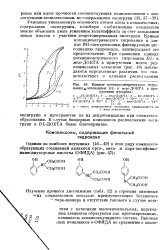 |
Кривые потенцпометрического титрования j основанием DL - к лезо - ДОБТА в присутствии иттербия. 1 - ЛЬ-ДОБТА. 1 - мезо - ДОБТА. 2 - ВГ. - ДОБТА. [9] |
В случае биядерных комплексов расположение оксигрупп в /) 1 - ДОБТА более благоприятно. [10]
При образовании биядерных комплексов этих металлов наблюдается диссоциация обеих оксигрупп. ДОБТА в присутствии двукратного количества меди образует как бы две равные ступени, и двум последовательным стадиям комплексообразования соответствуют примерно равные константы устойчивости комплексов. Это свидетельствует о том, что в биядерных комплексах переходных металлов, вероятно, образуются две самостоятельные, практически равноценные симметричные координационные сферы с координацией депротонированных гидр-оксилов. Наиболее ярко проявляется участие оксигрупп, сопровождающееся диссоциацией гидрокислов, при координации железа. [11]
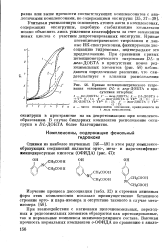 |
Кривые потенциометрического титрования основанием DL - и лезо - ДОБТА в присутствии иттербия. [12] |
В случае биядерных комплексов расположение оксигрупп в DL-ДОБТА более благоприятно. [13]
Кристаллическая структура последнего биядерного комплекса идентифицирована методом рентгеноструктурного анализа. [14]
В редких случаях образовавшийся биядерный комплекс может оказаться устойчивым, так что лимитировать весь процесс будет последняя стадия - распад этого комплекса. [15]
Страницы: 1 2 3 4