Сольватный комплекс
Cтраница 3
 |
Значения расщепления в кристаллическом поле ( Dqi для иона двухвалентного никеля в различных растворителях. [31] |
Если рассматривать сольватацию донорным растворителем как образование комплекса, экспериментально наблюдаемые устойчивости образованных сольватных комплексов с данным акцептором могут служить мерой донорнои способности растворителя. [32]
Следует предполагать, что ионы карбония в жидкой фазе сольватированы и представляют собой положительно заряженные сольватные комплексы. [33]
Опираясь на приведенные соображения, на основании энергий d - d - полос сольватных комплексов можно было бы построить спектро-химический [175] и нефелоксетический ряды растворителей. На самом деле, однако, это не так просто сделать, так как замена растворителя не полностью эквивалентна замене лиганда. В случае замены растворителя диэлектрическая проницаемость системы изменяется, что сопровождается изменением диссоциативного равновесия. Кроме того, растворитель в отличие от прочих лигандов, взаимодействует не только с катионом, но и с анионом. Замена растворителя может вызвать изменение в сольватации обоих ионов, что в свою очередь изменяет условия диссоциации. Последнее является причиной того, почему в аналогичных системах, содержащих анионы ( наряду с ионами металла), имеются исходный и смешанный сольваты различных составов в зависимости от донорно-акцепторных и диэлектрических свойств растворителя. Например, в водных растворах галогенидов двухвалентных переходных металлов металл присутствует в форме компг. При замене воды растворителем с более низкой диэлектрической проницаемостью ( например, ацетонитрилом) помимо растворителя в первую координационную сферу иона переходного металла входят также ионы галогенида. [34]
Показано, как взаимодействие мезогенной фосфолипидной молекулы и молекул оды образует структурный элемент ЛЖК - сольватный комплекс ( комбинированный свантовохимический и вероятностный расчеты): вычислены вероятности атом-атомных сонтактов; определены наиболее вероятные геометрические конфигурации сольватного ( омплекса; рассчитаны энергетические и спектроскопические характеристики данных сонфигураций. [35]
Экспериментальные данные показывают, что при сильном энергетическом взаимодействии между молекулами растворителя и полимера с образованием сольватных комплексов процесс растворения не всегда проходит до конца, останавливаясь на стадии ограниченного набухания. При сильном взаимодействии молекулы растворителя могут располагаться в строго упорядоченном состоянии по местам активных атомов или групп полимерных цепей, с которыми молекулы растворителя образуют сольватные комплексы. Следовательно, число микросостояний молекул растворителя резко снижается по сравнению с числом микросостояний их в самом растворителе. [36]
В настоящее время уравнения Борна и Борна - Бьеррума используют обычно для учета взаимодействия со средой сольватного комплекса. [37]
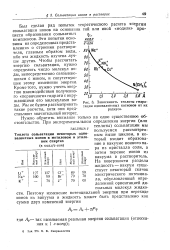 |
Зависимость теплоты гидратации одновалентных катионов от их. [38] |
Был сделан ряд попыток теоретического расчета энергии сольватации ионов на основании той или иной модели процесса образования сольватных комплексов. Эти попытки основаны на определенных представлениях о строении растворителя, главным образом воды, ибо эта жидкость изучена лучше других. Чтобы рассчитать энергию сольватации, нужно определить число молекул воды, непосредственно связывающихся с ионом, и сопутствующее этому изменение энергии. [39]
Для присоединения электрона ион должен быть поднят из глубокой потенциальной ямы, обусловленной низким уровнем потенциальной энергии сольватного комплекса. [40]
 |
Теплота гидратации ионов по данным К. П. Мищенко. [41] |
Был сделан ряд попыток теоретического расчета энергии сольватации ионов на основании той или иной модели процесса образования сольватных комплексов. [42]
Для присоединения электрона ион должен быть поднят из глубокой потенциальной ямы, обусловленной низким уровнем потенциальной энергии сольватного комплекса. [43]
 |
Стабильности ( 5 сольватов хлорида железа ( ПГ по отношению к сольватам с диметнлформа-мидом, донорная способность DN я диэлектрическая проницаемость Б соответствующих растворителей 417 ]. [44] |
Из проведенного краткого обзора можно видеть, что спектроскопия Мессбауэра полезно дополняет наши знания о сольватации и сольватных комплексах, полученные другими методами. Составы частиц в растворе можно определить с использованием различных методов изучения равновесий, и здесь мессбауэровский спектр в основном дает непрямую информацию. Однако мессбауэровская спектроскопия позволяет определять симметрию и электронную структуру частиц. В тех случаях, когда в сольватационном равновесии участвует мессбауэровский атом, спектр которого хорошо разрешен, этот метод можно использовать и для изучения равновесий в классическом смысле. [45]
Страницы: 1 2 3 4