Спиральный комплекс
Cтраница 1
Спиральные комплексы устойчивы к ферментативному фосфоро-лизу [83], в то время как менее упорядоченные или неупорядоченные структуры при определенных условиях разрушаются. [1]
У полинуклеотидов и спиральных комплексов, кроме гипохромизма при Ямакс, возникающего в результате упаковки друг над другом л-л хромофорных единиц, гиперхромный эффект проявляется и при более длинных длинах волн. Такое увеличение оптического поглощения ( при 280 - 300 мц) замечено у нескольких спиральных полинуклеотидных комплексов. [2]
По многим свойствам такой спиральный комплекс напоминает ДНК. Так, у него обнаружены явления молекулярного плавления, или перехода спираль - клубок. Одновременно значительно уменьшается специфическое оптическое вращение при 589 ммк. [3]
Далее оказалось, что простые полинуклеотидные цепочки обладают способностью давать значительно большее разнообразие спиральных комплексов, чем природные сополимеры сложного состава. Так, цепи составленные из одних пиримидиновых поли-нуклеотидов, дают спиральные комплексы сами с собой. [4]
Однако при подкислении до рН 4 5 происходит немедленная агрегация, вероятно вследствие разрушения спирального комплекса протежированием цитозиновых остатков. Результаты позволили предположить довольно заметную гетерогенность состава ( или, возможно, структуры) транспортных нуклеиновых кислот. [5]
Энтальпия, рассчитанная на моль иода ( в виде I), систематически увеличивается при добавлении в спиральном комплексе мальтодекстрина каждой следующей глюкозной структурной единицы. Очевидно, самое низкое значение степени полимеризации, при котором происходит максимальное взаимодействие первичного триио-дид-иона, входящего в амилозную спираль, является таким же, которое необходимо для получения окраски в растворах комплекса. [6]
Прерывность AG для реакции образования комплекса при Р 6 - f - 7 ( см. рис. 184) объясняется переходом от петлеобразного к спиральному комплексу. [7]
При соотношении А: У 2: 1 наблюдалось максимальное уменьшение оптического поглощения ( 35 %), что указывало на образование комплекса, сходного с трех-цепочечным спиральным комплексом, содержащим две цепи полиуридиловой и одну цепь полиадениловой кислот ( см. стр. [8]
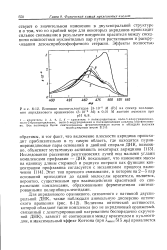 |
Влияние полинуклеотидов [ 3 - 10 - 5 М ( Р ] на спектр поглощения акридинового оранжевого ( 3 - 10 - 5 М в 0 01 М ацетате аммония при. [9] |
Этот тип прочного связывания, в котором на 2 - 5 пар оснований приходится до одной молекулы красителя, является, вероятно, существенным при взаимодействии красителей со спиральными комплексами, образованными ферментативно синтезированными полирибонуклеотидами. [10]
После более детального изучения поляризованных спектров ориентированных пленок двухспиральных сополимеров ( дезокси-аденилил-тимидиловой кислоты) [384] тот факт, что именно л - я переход приводит к появлению гиперхромной полосы при 280 мр в спиральных комплексах типа полиаденилил-полиуридиловой кислоты [381], был подвергнут серьезному сомнению. [11]
Далее оказалось, что простые полинуклеотидные цепочки обладают способностью давать значительно большее разнообразие спиральных комплексов, чем природные сополимеры сложного состава. Так, цепи составленные из одних пиримидиновых поли-нуклеотидов, дают спиральные комплексы сами с собой. [12]
Больц-мана, е - заряд электрона, N - число Авогадро, / - ионная сила. При ионной силе / 0 1 толщина становится порядка 10 А, что достаточно для нейтрализации кулоновского отталкивания между цепями и образования ими спирального комплекса. Из рис. 68 видно, что при эквимолекулярном составе смеси получается острый минимум оптической плотности или наибольший гипохром-ный эффект. [13]
Последнее сказывается на длине углеродной цепи, а следовательно, на образовании спирали и включении молекул иода. Внешние ответвления молекул длиннее внутренних, которые образуют сегменты цепи, лежащие между точками ответвлений. Длина внешних ответвлений в амилопектине колеблется от 14 до 17 глюкозных структурных единиц в зависимости от природного источника, а в более разветвленном гликогене [2, 55] - от 4 до 11, и их средняя длина также зависит от происхождения гликогена. Длина внутренних ветвей колеблется от 5 до 8 глюкозных структурных единиц в амило-пектинах и от 2 до 7 - в гликогенах. Так как амилопектин и гликоген можно считать статистическими полимерами [27], то следует ожидать, что средняя длина ответвлений будет разной и некоторые ответвления в гликогене и амилопектине по длине превысят 18 глюкозных структурных единиц, что так необходимо для появления окраски в спиральных комплексах. [14]
Страницы: 1