Последний комплекс
Cтраница 3
Две молекулы воды в последнем комплексе занимают наиболее удаленные от центрального иона меди положения в тетрагональной бипирамиде. Ассиметрия этих полос, возможно, связана с тем, что они состоят по меньшей мере из двух сильно перекрывающихся полос. [31]
Среднее расстояние - Pt-Me в последнем комплексе равно 2 05 А; расстояния Pt-N 2 15 А близки к найденным в описанном выше 8-окси-хинолинате териметилплатины. Связь Pt-Сдсас 2 38 А ослаблена, по-видимому, наиболее резко; обратного трамс-влияния на метальную группу, расположенную я а той же координате комплекса, она не оказывает. [32]
Приведенные выше уравнения показывают, что для последнего комплекса зависимость F / от [ X ] выражается прямой параллельной оси концентраций. [33]
Приведенные выше уравнения показывают, что для последнего комплекса зависимость FJ от [ X ] выражается прямой параллельной оси концентраций. [34]
Из иодидных растворов экстрагируются CuJ2 и Cu2J3, причем последний комплекс, по их данным, сольва-тирован тремя молекулами ТБФ. Экстракция хлороформом хлоридного комплекса меди ( 1) в присутствии ДАПМ применена для аналитического определения меди в смеси с железом, скандием и редкоземельными элементами. [35]
Поскольку рассматривается течение пара с заданной скоростью, то все величины, из которых составлен последний комплекс, входят в условия однозначности и, следовательно, это критерий определяющий. Он представляет собою меру отношения силы трения пара о пленку к силе тяжести. [36]
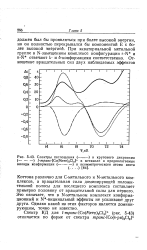 |
Спектры поглощения ( - - - - - - - - и кругового дихроизма. [37] |
Коттона различно для С-метильного и N-метильного комплексов, а вращательная сила доминирующей положительной полосы для последнего комплекса составляет примерно половину от вращательной силы для первого. Это означает, что в N-метильном комплексе конформа-ционный и М - вицинальный эффекты не усиливают друг друга. Однако какой из этих факторов является доминирующим, точно не известно. [38]
Таким образом получают обе константы равновесия kn и & п-то, а также коэффициенты поглощения Е, еп-т и е т-р трех последних комплексов с максимальным числом лигандов X, приходящихся на ион металла. [39]
При 35 С обмен в случае первых двух комплексов протекал медленно ( период полуобмена 5 7 часа), а в случае двух последних комплексов - - быстро ( период полуобмена 6 сек. [40]
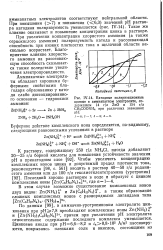 |
Катодные поляризационные кривые в аммиакатном электролите, содержащем 14 г / л ZnO и 154 г / л CH3COONH4 при различных значениях рН. / - 6. 2 - 7. 3 - 8. 4 - 9. [41] |
По данным [99], в аммиачно-уротропиновом электролите цинкования при рН 7 8 преобладают комплексные ионы Zn ( NH3) и [ Zn ( NH3) 3C6Hi2N4 ] 2, причем при увеличении рН электролита относительное содержание последнего комплекса уменьшается. [42]
Молекула хлорного хрома, существующего в трех формах, может быть представлена в виде координационных групп [ Си ( Н2О) 4 ] С1, [ Сг ( Й2О) 5 ] С12 и [ Сг ( Н2О) е ] С1з; причем последний комплекс диссоциирует на катион ( фиолетового цвета) и три иона СГ -, вследствие чего он обладает в водном растворе значительной электропроводностью. [43]
Для выполнения работ первого уровня необходима система самого низкого, базового уровня с возможными вариациями. Последний комплекс для выполнения работ третьего уровня уже никак нельзя назвать ни персональным, ни настольным. Для него понадобится специализированное оборудование и программы, но нужно подчеркнуть, что каждый последующий уровень включает предыдущий с необходимыми расширениями и дополнениями, причем в структуре этих работ содержатся рабочие места как первого, так и второго уровней. [44]
При малых кинетических энергиях сталкивающихся молекул они могут образовывать димеры, стабилизируемые межмолекулярными силами. Последние комплексы стабилизируются в основном дисперсионными силами, поэтому их иногда называют ван-дер-ваальсо-выми молекулами [84, 85], подчеркивая тем самым их отличие от молекул с обычной химической связью. В данном пункте мы кратко рассмотрим свойства ваи-дер-ваальсовых комплексов, а также комплексов, образуемых при переходе молекулы в электронно-возбужденное состояние, в следующем пункте остановимся на свойствах комплексов с водородной связью. [45]
Страницы: 1 2 3 4