Хлоридный комплекс - висмут
Cтраница 1
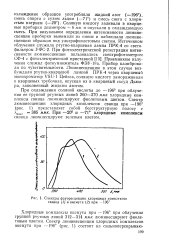 |
Спектры флуоресценции хлоридных комплексов свинца (. и висмута ( 2 при - 196. [1] |
Хлоридные комплексы висмута при - 196 при облучении группой ртутных линий 312 - 314 ммк люминесцируют фиолетовым цветом. [2]
Ни китенке Т. Ф. Потенциометрическое исследование хлоридных комплексов висмута / / Журн. [3]
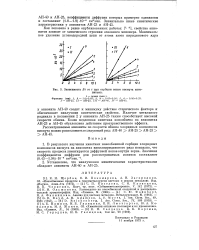 |
Зависимость Bt от t при сорбции ионов висмута анио. [4] |
В результате изучения кинетики ионообменной сорбции хлоридных комплексов висмута на анионитах винилпиридинового ряда показано, что скорость процесса лимитируется диффузией ионов внутри зерна. [5]
 |
Кинетические кривые сорбции ионов висмута в зависимости от крупности зерен анионитов. [6] |
В настоящей работе приводятся результаты исследований по кинетике ионного обмена хлоридных комплексов висмута на анионитах винилпи-ридинового ряда: АН-23, АН-25, АН-40, АН-45. Рассматриваемые анио-ниты получены сополимеризацией 2-винилпиридина ( АН-23), 2-метил - 5-винилпиридина ( АН-25), 4-винилпиридина ( АН-40), 2 - Ш - диметиламино-этил ] - 5-винилпиридина ( АН-45) с 8 % дивинилбензола. [7]
Как было отмечено выше, чистый хлороформ и ряд других органических растворителей не извлекает хлоридных комплексов висмута. Очевидно, экстракция аминами может происходить лишь в связи с образованием анионных хлоридных комплексов. [8]
Для определения висмута использована 20 % - ная бромистоводородная кислота и найден минимум свето-поглощения при 373 мц. Хлоридный комплекс висмута имеет максимальное светопоглощение при ЗЗОжц, но он малопригоден для определения. [9]
Перспективным является определение висмута в растворе соляной кислоты при замораживании раствора жидким азотом. Было показано351, что хлоридные комплексы висмута при - 196 С и облучении группой линий ртути 313 - 314 ммк люминесцируют фиолетовым цветом. Спектр люминесценции хлоридных комплексов висмута при - 196 С состоит из сильно перекрывающихся полос с лшах около 410 ммк. При охлаждении до - 20 С хлоридные комплексы висмута не люминесцируют, при охлаждении до - 71 СС - люминесценция чрезвычайно слаба. [10]
Перспективным является определение висмута в растворе соляной кислоты при замораживании раствора жидким азотом. Было показано351, что хлоридные комплексы висмута при - 196 С и облучении группой линий ртути 313 - 314 ммк люминесцируют фиолетовым цветом. Спектр люминесценции хлоридных комплексов висмута при - 196 С состоит из сильно перекрывающихся полос с Хтах около 410 ммк. При охлаждении до - 20 С хлоридные комплексы висмута не люминесцируют, при охлаждении до - 71 С-люминесценция чрезвычайно слаба. [11]
Предложен расчетный способ определения необходимой для экстракции металлов аминами концентрации галоге-нид-ионов с использованием констант нестойкости. Соответствие теоретических расчетов и экспериментальных исследований подтверждается примером экстракции хлоридных комплексов висмута и цинка. [12]
Как сказано выше, интенсивность люминесценции хлоридных комплексов свинца при понижении температуры резко увеличивается, а хлоридные комплексы висмута люминесцируют вообще только при низких температурах. [13]
Из солей Bi111 легче всего гидролизуется хлорид; затем идут нитрат, перхлорат. Гидролизуемость В1С13 в растворах уменьшается при повышении концентрации ионов Н и С1 - ( добавление хлоридов щелочных металлов) вследствие образования хлоридных комплексов висмута. При понижении кислотности растворов BiCl3 и Bi ( NO3) 3 выделяются белые осадки основных хлоридов и нитратов. [14]
В люминесцентном анализе с успехом может быть использована флуоресценция комплексных соединении с неорганическими алдендами. При облучении соляной кислоты, охлажденной до минус 196 и содержащей ионы свинца, ртутной линией 272 ммк наблюдается флуоресценция фиолетового цвета. Хлоридные комплексы висмута флуоресцируют тоже фиолетовым цветом при облучении группой ртутных линий 312 - 314 ммк. Спектр флуоресценции хлоридных комплексов свинца при минус 196 представляет бесструктурную полосу с максимумом 385 ммк, а висмута - - 410 ммк. Резкое увеличение выхода флуоресценции хлоридных и бромидных комплексов ряда катионов при низких температурах ( а в некоторых случаях и в сорбированном состоянии) делает возможным определение этих элементов без предварительной обработки ее химическими реактивами. [15]
Страницы: 1 2