Различный комплекс
Cтраница 2
При рассмотрении различных комплексов платины ( IV), отличающихся лишь природой координированных аминов, выяснилось, что равновесие амидореакции сдвигается в правую сторону в тем большей степени, чем более основными свойствами обладает амин в некоординированном состоянии. Например, этиленди-аминовые комплексы имеют в растворе более кислую реакцию чем аммиачные комплексы. Сравнение констант кислотной диссоциации диэтилендиамминодихлоро - и тетрамминодихлоросое-динений показывает, что здесь наблюдается отступление от этой закономерности. [16]
Если последовательно образуются различные комплексы металл - индикатор, то необходимо учитывать концентрацию индикатора, связанного с металлом. [17]
Этими катализаторами оказались различные комплексы нульвалентного никеля, в особенности бисакрилонитрилникель и фосфиновые производные карбонила или цианида никеля. [18]
Железо в виде различных комплексов также обладает каталитическим действием, хотя реакции этих комплексов еще не настолько подробно исследованы, чтобы можно было установить механизм. При общем обсуждении процесса катализа действием комплексов железа Баксендейл [73] указал, что во время образования этих комплексов в присутствии перекиси водорода наблюдается более быстрое каталитическое разложение, чем разложение, которое происходит в присутствии одного трехвалентного железа или на следующей стадии, когда действует только один комплекс. Сделано заключение, что и в этом случае разложение происходит по свободиорадикальному механизму. Представляет интерес изучение разложения перекиси водорода цианидными комплексами железа [73, 264], поскольку это разложение зависит от действия излучения. Кистя-ковский [265] сделал наблюдение, что слабый каталитический эффект смеси феррсцианида с феррицианидом существенно увеличивается под действием света и что высокая скорость разложения сохраняется и после прекращения освещения. Срикантан и Рао [266] считают, что в этом катализе принимает участие комплекс, содержащий молекулу перекиси водорода, а результаты подробного исследования, проведенного Лалом [267], доказали важное значение, которое имеет в механизме реакции водный комплекс, образующийся при гидролизе цианида. Эта работа показывает также, что гидрат окиси железа не может функционировать в этом катализе в качестве активной частицы. [19]
Зная константы нестойкости различных комплексов, можно теоретически вычислить концентрацию соответствующих простых ионов в растворах комплексных солей. [20]
Из исследованных нами различных комплексов наиболее прочными являются цианидные. Это в значительной мере обусловлено силой поля ионов цианида, которая значительно выше, чем, например, ионов хлора. Однако в цианистых электролитах катодная поляризация часто меньше, чем в растворах других комплексов. [21]
Экономические проблемы создания различных комплексов являются в настоящее время наиболее сложными и мало исследованными в системе работ по размещению химической промышленности. [22]
Оптимальная каталитическая активность различных комплексов BF3 - амин проявляется при различных температурах. [23]
Характерная особенность интеграции различных комплексов заключается в том, что согласование их расчетов достигается отношениями директив сверху и предложений снизу. При этом обмен мнениями происходит между комплексом и подчиненным ему ЭО. Ранее уже подчеркивалось, что центральным моментом создания интегрированной АСОУ следует считать постановку сквозных комплексов задач по уровням планирования. Рассмотрим некоторые аспекты решения сквозных комплексов задач, имея в виду, что аналогичный подход может быть распространен на другие комплексы задач. Предположим, что в подсистеме Планирование производства комплекса К4 должна быть решена комплексная задача Формирование плановых заданий по выпуску изделия в союзной номенклатуре. [24]
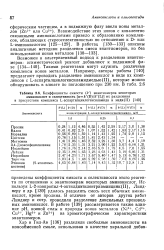 |
Коэффициенты емкости ( & энантиомеров некоторых. [25] |
Такими реагентами могут служить различные комплексы ионов металлов. Например, авторы работы [140] предлагают проводить разделение аминокислот в виде их комплексов с Ь - аспартилциклогексиламидмедью ( П), которые можно обнаруживать в элюате по поглощению при 230 нм. [26]
В табл. 1.13 для различных комплексов приведены величины А, определенные из спектров поглощения, вычисленные значения Р и данные о спиновом состоянии иона, полученные по результатам исследования магнитных свойств соединений. Как видно, приведенные в табл. 1.13 сведения находятся в соответствии с вышеизложенным. [27]
Зная величину констант нестойкости различных комплексов, можно теоретически вычислить концентрацию соответствующих простых ионов в растворах комплексных солей. Сказанное иллюстрируется следующими числовыми примерами. [28]
В табл. 1.13 для различных комплексов приведены величины А, определенные из спектров поглощения, вычисленные значения Р и данные о спиновом состоянии иона, полученные по результатам исследования магнитных свойств соединений. Как видно, приведенные в табл. 1.13 сведения находятся в соответствии с вышеизложенным. [29]
 |
Расщепление d - AO в октаэдриче. [30] |
Страницы: 1 2 3 4