Комплексообра-зователь
Cтраница 2
Очень часто ионы маскируют, добавляя подходящий комплексообра-зователь, который сам может быть фоном, или сдвигают в нужном направлении потенциал полуволны путем комплексообразования. [16]
Железо, кобальт и никель являются хорошими комплексообра-зователями. Железо и кобальт в степени окисления ( III) образуют в большинстве случаев октаэдрические комплексы, а кобальт в степени окисления ( II, d) - тетраэдрические и октаэдрические. [17]
В связи с этим были исследованы и другие комплексообра-зователи ( SbBi s, а-замещенные бензиламины, гидроксибензоат аммония), но они пока не нашли практического применения. [18]
В цианистых электролитах для золочения в качестве комплексообра-зователя рекомендуется отдавать предпочтение цианистому калию. [19]
Особенно большое значение для прочности связи с комплексообра-зователем того или иного лиганда имеет природа лиганда, находящегося в транс-положении к первому. Этот принцип транс-влияния лиганда очень важен для химии комплексных соединений платины и некоторых других металлов, так как дает возможность предугадывать порядок протекания реакций замещения в неоднородной внутренней сфере и позволяет сознательно выбирать пути синтеза желательных пространственно-изомерных форм вещества заданного состава. [20]
Для разделения меди и кадмия применяют в качестве комплексообра-зователя тиомочевину CS ( NH2b или цианистый калий. Это комплексообра-зователи связывают ( маскируют) ионы меди настолько прочно, что сероводород не осаждает сернистой меди. [21]
Такие же явления происходят в случае применения ряда комплексообра-зователей для удержания в растворе некоторых катионов. В качестве ком-плексообразователей часто применяют, например, винную кислоту СООН - СНОН-СНОН-СООН. Прочность виннокислых комплексов также зависит от рН раствора. При понижении кислотности катион более прочно связывается с анионом винной кислоты. Поэтому некоторые ионы, например тантала и ниобия, осаждаются оксихинолином в присутствии виннокислых солей только при подкислении растворов. Наконец, многие органические реактивы в сильнощелочной среде могут довольно быстро окисляться кислородом воздуха; при этом образуются новые соединения, и условия осаждения нарушаются. [22]
Лиганды, расщепляя уровни энергии d - электронов комплексообра-зователя, в свою очередь сами испытывают влияние со стороны его электронов, не участвующих в связях. Это проявляется в их отталкивании от центра комплекса, в искажении его структуры. Лишь при равномерном заполнении электронами d - орбиталей одного и того же типа ( de и dy) симметрия электронной плотности вокруг комплексооб-разователя не вызывает изменений в правильных структурах. Данные табл. 24 показывают, какое число d - электронов у комплексообразова-теля, находящегося в слабых и сильных полях лигандов, необходимо для образования правильных октаэдрических и тетраэдрических комплексов. Все другие электронные конфигурации должны приводить к искаженным октаэдрам и тетраэдрам. [23]
Для разделения меди и кадмия применяют в качестве комплексообра-зователя тиомочевину CS ( NH2) 2 или цианистый калий. Эти комплексообра-зователи связывают ( маскируют) ионы меди настолько прочно, что сероводород не осаждает сернистой меди. [24]
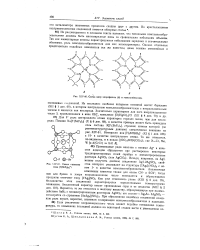 |
Схема яле -. р хлорофилла ( Л и гемоглобина ( В.| Схема строения иона [ F ( SbF3 4J -. [25] |
Из рассмотренного в основном тексте вытекает, что типичными комплексообра-зователями должны быть многозарядные ионы со сравнительно небольшим объемом. Так как элементарные анионы характеризуются небольшими зарядами и значительными объемами, роль комплексообразователя для них малохарактерна. [26]
Комплексные соединения образуются донорно-акцеп-торным способом за счет присоединения комплексообра-зователем определенного числа других ионов, молекул или радикалов, именуемых лигандами. Наиболее распространенными следует считать следующие лиганды: анионы - С1 -, CN -, SO -, ОН, О -, NH2 -, NH -, SCN -; нейтральные - Н2О, NH3, CO, NO. В качестве атомов-комплексо-образователей могут быть нейтральные и заряженные частицы. Нейтральными комплексообразователями служат атомы многих элементов побочных подгрупп V, VI, VII, VIII групп периодической системы. [27]
Нормальному протеканию осадительных процессов мешает присутствие в очищаемых водах комплексообра-зователей ( фтористые соли, оксалаты, сульфонафтеновые препараты и др.), мыла и других моющих средств, попадающих туда с водами санпропускников и спецпрачечных. [28]
Приведите примеры комплексных соединений элементов восьмой группы, в которых комплексообра-зователь проявляет нулевую валентность. [29]
Благодаря этому электронная пара иона J - сильнее смещается к комплексообра-зователю. [30]
Страницы: 1 2 3 4