Заметное комплексообразование
Cтраница 1
Заметное Комплексообразование происходит через 6 - 8 мин от начала перемешивания. [1]
Первоначально предполагалось, что это постоянство потенциала указывает на отсутствие заметного комплексообразования между Се ( IV) и Ж) 3-ионами, однако, согласно новым данным, можно допустить образование некоторого количества Ce ( NO3) 6 - - ионов. [2]
Если комплексы неустойчивы ( сильно диссоциируют), то для заметного комплексообразования концентрация лигандов Сх должна быть очень велика по сравнению с CM. Тогда изменением концентрации лигандов вследствие комплексообразования практически можно пренебречь. [3]
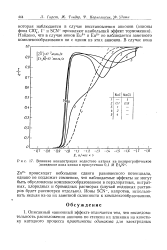 |
Влияние концентрации йодистого натрия на полярографическое. поведение иона цинка в присутствии 0 1 М. Et4N. [4] |
Найдено, что в случае ионов Еи3 и Еи2 не наблюдается заметного комплексообразования ни с одним из этих анионов. [5]
КУ-2 и 0 125 М раствором хлорной кислоты, что указывает на отсутствие заметного комплексообразования. [6]
Установлено, что при изменении концентрации НСЮ4 от 1 до 10 М не происходит заметного комплексообразования Np j ( IV) с перхлоратными ионами. [7]
Спектр поглощения Np ( V) в 1 М EbSOi идентичен спектру поглощения перхлоратного раствора, что свидетельствует об отсутствии заметного комплексообразования с сульфат-ионами при данной концентрации. [8]
Среди дикарбоновых кислот щавелевая дает наиболее прочные комплексные соединения с цирконием и гафнием. Гомологи щавелевой кислоты - малоновая ( 0 03 М), янтарная ( 0 2 М) и глутаровая ( 0 1 М) кислоты не изменяют коэффициента распределения Zr4 и Ш4 на катионите в 0 125 М растворе НС1О4, что указывает на отсутствие заметного комплексообразования в этих системах. [9]
Среди дикарбоновых кислот щавелевая дает наиболее прочные комплексные соединения с цирконием и гафнием. Гомологи щавелевой кислоты - малоновая ( 0 03 М), янтарная ( 0 2 М) и глутаровая ( 0 1 М) кислоты не изменяют коэффициента распределения Zr4 и Hf4 на катионите в 0 125 М растворе НС1О4, что указывает на отсутствие заметного комплексообразования в этих системах. [10]
На рис. 7 - 2 представлены данные растворимости хлорида серебра, графически иллюстрирующие [15] минимальную растворимость, влияние общего иона и собственную растворимость S, a также образование хлорсодержащих комплексов. Как видно из рис. 7 - 26, при низких концентрациях избыточного хлорида наблюдается действительно линейная зависимость между растворимостью и величиной, обратной произведению концентрации ионов хлорида и квадрата коэффициента активности. Поскольку при низких концентрациях ионов хлорида заметного комплексообразования не происходит, лишь первые два члена в уравнении ( 7 - 33) имеют значение. [11]
Существуют ионы металлов, образующие устойчивые комплексонаты, присутствие которых тем не менее не мешает титрованию других металлов, потому что эти ионы очень медленно реагируют с комплексообразующим веществом. Такие ионы Рейли метко назвал кинетически замаскированными. Смесь хрома ( III) и ЭДТА оставляют на продолжительное время, для того чтобы произошло заметное комплексообразование. [12]
Страницы: 1