Компонент - бинарная система
Cтраница 4
 |
Возникновение области концентрационного переохлаждения ( на рисунке заштрихована. [46] |
Линии ликвидуса, представляющие собой в то же время кривые температурной зависимости растворимости соответствующего вещества в расплаве второго компонента бинарной системы [41], сходятся в точке Е, называемой эвтектической точкой. Расплав отвечающего ей состава затвердевает при постоянной температуре ТЕ, образуя мелкодисперсную механическую смесь фаз А и В - эвтектику. При охлаждении расплавов иного состава вначале кристаллизуется только А ( слева от точки Е) или только В ( справа от нее), и лишь по достижении температуры ТЕ происходит затвердевание оставшегося расплава в виде эвтектики. Следовательно, в случае состава, отвечающего точке F на рис. 112, образование кристаллов вещества А происходит в интервале от TF до ТЕ. [47]
Физическое титрование ( чаще всего водой) основано на малой растворяющей способности титранта по отношению к одному из компонентов жидкой бинарной системы при высокой растворимости второго компонента. [48]
Наибольшее распространение получили системы с положительными отклонениями от идеального поведения, в которых Y 1 - Экспериментальные зависимости коэффициентов активности компонентов бинарной системы от состава обычно выражается параболическими кривыми, пересекающимися в эквимолекулярной области. [49]
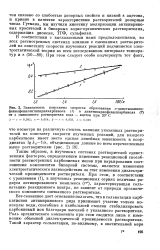 |
Зависимость константы скорости образования п-диметиламино-фенилфенилантипирилкарбинола ( 1 и диантипирилфенилкарбинола ( 2 от е смешанного растворителя вода - ацетон при 20 С. [50] |
Таким образом, в изученных системах растворителей единственным фактором, определяющим изменение реакционной способности рассмотренных карбониевых ионов при варьировании соотношения компонентов бинарной системы, является изменение электростатического взаимодействия за счет изменения диэлектрической проницаемости растворителя. При этом, в соответствии с уравнением ( 1), в изученных реакционных сериях величина радиуса активированного комплекса ( г), характеризующая сольватацию реакционного центра, не зависит от природы органического компонента смешанного растворителя. [51]
Из уравнения ( 123) вытекает, что эффективное действие таких разделяющих агентов возможно в тех случаях, когда отношение давлений паров компонентов заданной бинарной системы достаточно велико. Указанные разделяющие агенты могут быть применены в частности для разделения систем, компоненты которых, несмотря на большую разницу температур кипения, образуют азеотропы или в определенной области концентраций имеют состав пара, мало отличающийся от состава жидкости. Отсюда вытекают следующие положения, на основании которых должен производиться выбор разделяющих агентов. [52]
Из уравнения ( 126) вытекает, что эффективное действие таких разделяющих агентов возможно в тех случаях, когда отношение давлений паров компонентов заданной бинарной системы достаточно велико. Указанные разделяющие агенты могут быть применены, в частности, для разделения систем, компоненты которых, несмотря на большую разницу температур кипения, образуют азеотропы или в определенной области концентраций имеют состав пара, мало отличающийся от состава жидкости. Отсюда вытекают положения, на основании которых следует производить выбор разделяющих агентов. [53]
Из уравнения ( 123) вытекает, что эффективное действие таких разделяющих агентов возможно в тех случаях, когда отношение давлений паров компонентов заданной бинарной системы достаточно велико. Указанные разделяющие агенты могут быть применены в частности для разделения систем, компоненты которых, несмотря на большую разницу температур кипения, образуют азеотропы или в определенной области концентраций имеют состав пара, мало отличающийся от состава жидкости. Отсюда вытекают следующие положения, на основании которых должен производиться выбор разделяющих агентов. [54]
Этот метод требует экспериментального определения давления пара и температур кипения чистых веществ и смесей, содержащих / з и 2 / з молярных доли каждого компонента бинарной системы. [55]
В некотором роде исключением можно считать те реакции, в которых образование комплекса происходит между радикалом и молекулой реагента, выступающего часто в качестве растворителя или компонента бинарной системы. Однако наблюдаемые в таких реакциях закономерности не следует, вероятно, связывать с чисто сольватационными эффектами. Действительно, если между радикалом R - и реагентом ( растворителем) RH образуется комплекс за счет водородной связи, то этот комплекс является по-существу заготовкой переходного состояния. Ускорение реакции в таких системах вполне закономерно. К сожалению, экспериментальных данных для детального исследования этого вопроса совершенно недостаточно. [56]
Страницы: 1 2 3 4