Компонент - газовая смесь
Cтраница 3
Разделение компонентов газовой смеси в газо-жидкостной хроматографии основано на их различном распределении между неподвижной жидкой фазой и подвижной газообразной. [31]
Для компонента газовой смеси, как уже говорилось, G относится к состоянию с р атм. Если воспользоваться парциальным давлением, выраженным в Па, то нельзя применять (14.9), а нужно воспользоваться (14.22), подставляя в него р 1 013 - 105 Па. Если же сохранить выражение (14.9) в системе СИ, то в качестве G следует принять значение G / при р1 Па. [32]
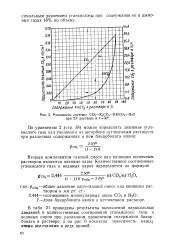 |
Равновесие системы СО2 - К2СО3 - КНСО3 - Н2О при 2N растворе и 30. [33] |
Вторым компонентом газовой смеси над кипящим щелочным раствором являются водяные пары. [34]
Если какой-либо компонент газовой смеси поглощается раствором, необходимо знать его коэффициент маесопереноеа. Для удаления твердых частиц требуется их физическая характеристика: распределение по размерам, плотность и форму. Важно также знать, являются ли частицы хорошим проводником или каковы их магнитные свойства. [35]
Теплопроводность остальных компонент газовой смеси не влияет на показания прибора; однако показания зависят от вязкости и теплоемкости газовой смеси. Вязкость влияет на скорость движения газового потока в горизонтальной трубке, а теплоемкость определяет количество тепла, передаваемого от трубки к газу. Для большинства случаев анализа на кислород эти погрешности невелики. [36]
Тяжелые же компоненты газовых смесей иногда удаляются с помощью абсорбции. [37]
Объемная концентрация компонентов газовой смеси приблизительно равна концентрации но молям ( V %), yh поскольку объемы I киломоля идеального газа при одинаковых физических условиях по закону Авогадро ( см. подразд. [38]
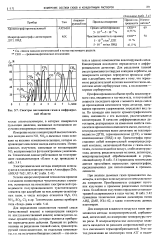 |
Спектры поглощения газов в инфракрасной области. [39] |
Для определения компонентов газовой смеси ( качественный анализ) и концентрации каждого из них ( количественный анализ) используются газовые хроматографы, которые являются приборами периодического действия. [40]
Парциальное давление компонента газовой смеси представляет собой то давление, которое он оказывает при удалении из объема, занимаемого смесью, остальных компонентов при неизменных первоначальных объеме и температуре. [41]
Химический потенциал компонента газовой смеси был выражен, как обычно, через частную производную свободной энергии смеси по числу молей компонента. В свою очередь для свободной мольной энергии смеси было использовано выражение, выведенное при помощи статистической механики. [42]
Парциальное давление компонента газовой смеси представляет собой то давление, которое оказывает он один при удалении из объема, занимаемого смесью, остальных компонентов при неизменных первоначальных объеме и температуре. [43]
Зная теплоемкости компонентов газовой смеси и вычислив ее теплоемкость, из материального баланса процесса можно определить значения m и Q с учетом степени конверсии аммиака. Отсюда находят повышение температуры At вследствие выделения тепла реакции. [44]
 |
К выводу уравнения массопередачи для примера IX-3.| Схема массопередачи на эле-ментарном участке ЬХ. [45] |
Страницы: 1 2 3 4