Любой компонент - смесь
Cтраница 2
Последнее уравнение является общим выражением для взаимного пересчета весовых, мольных и объемных долей любого компонента смеси. [16]
Дальтона - Рауля, согласно которому можно сделать важный вывод - в состоянии равновесия парциальное давление любого компонента смеси в паровой фазе равно парциальному давлению того же компонента в жидкости. [17]
До настоящего времени нет достаточно четкого объяснения того, почему улучшается растворяющая способность смеси растворителей по сравнению с любым компонентом смеси. [18]
Идеальными растворами называются жидкие смеси, чье поведение подчиняется закону Рауля, согласно которому при постоянных температуре и давлении парциальное давление пара любого компонента смеси находится в постоянном отношении к его молярной доле. [19]
При работе по вытеснительному методу движение компонентов вдоль колонки происходит под действием газа-вытеснителя, в качестве которого может быть применено соединение, сорбирующееся или растворяющееся лучше любого компонента смеси. [20]
Преимущество хроматографического метода перед химическим в том, что он дает не только количественную, но и качественную информацию и позволяет, в случае необходимости, определить любой компонент смеси газов, образующейся при разложении неорганического продукта. [21]
В вытеснительной хроматографии некоторое количество более или менее разбавленной пробы вводится в колонку и поток газа-носителя немедленно заменяется потоком смеси этого газа и пара, который взаимодействует с неподвижной фазой более сильно, чем любой компонент смеси. Этот пар вытесняет пробу впереди себя, и каждый компонент этой пробы вытесняет компоненты, которые взаимодействуют менее сильно с неподвижной фазой, чем он сам. На выходе из колонки происходит последовательное элюирование зон компонентов смеси. Эти зоны следуют близко друг за другом, и соседние зоны несколько перекрываются. Для правильного проведения вытеснения требуется относительно большая концентрация пробы. По этим причинам данный метод больше подходит для препаративных, чем для аналитических, применений. Кроме того, прежде, чем может быть проведен второй цикл разделения, требуется регенерация колонки с удалением вытеснителя. Это может занимать значительное время. [22]
При выборе газа-носителя необходимо учитывать следующие требования: 1) инертность по отношению к разделяемому веществу, адсорбенту и неподвижной фазе; например, при анализе непредельных углеводородов не рекомендуется использовать в качестве газа-носителя водород, который, особенно если анализ ведется при повышенных температурах, может привести к гидрированию углеводородов; 2) поглощение сорбентом или растворение в неподвижной фазе значительно меньше любого компонента смеси ( это условие обязательно для проявительного анализа); 3) минимальная вязкость для обеспечения невысокого перепада давлений в колонке; 4) высокий коэффициент диффузии; 5) обеспечение высокой чувствительности применяемого детектора; 6) безопасность и достаточная чистота. [23]
Каждая ступенька отвечает чистому компоненту, и количество выделенного чистого компонента на колонке может быть определено по кривой разгонки. Общее суммарное количество любого компонента смеси включает вещество, отвечающее и тем частям излома кривой, которые показаны S-образными переходными линиями между ступеньками. В качестве первого приближения количество компонента в переходной фракции может быть установлено, если провести вертикальную линию в точке, находящейся посередине между началом одной ступеньки и концом соседней ступеньки, отвечающими следующим друг за другом нижекипящим и вышекипящим компонентам. Для многих практических целей результаты анализа, полученные этим методом, достаточно точны. Если же требования к анализу повышенные, можно воспользоваться другими способами для определения состава переходных фракций. Эти методы будут рассмотрены ниже. [24]
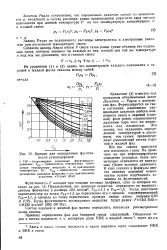 |
Кривые для определения фугитив. [25] |
Уравнение ( 3) известно под названием объединенный закон Дальтона - Рауля о равновесии фаз. Формулируется он так: в состоянии равновесия парциальное давление любого компонента смеси в паровой ( газовой) фазе равно парциальному давлению пара того же компонента над жидкостью. Это значит, что задавшись определенной температурой и давлением, тем самым предопределяют равновесный состав паровой и жидкой фаз. [26]
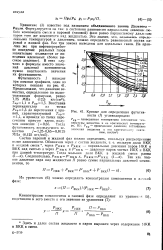 |
Кривые для определения фугитивности ( f углеводородов. [27] |
Уравнение ( 3) известно под названием объединенного закона Дальтона - Рауля. Формулируется он так: в состоянии равновесия парциальное давление любого компонента смеси в паровой ( газовой) фазе равно парциальному давлению паров того же компонента нал жидкостью. Это значит, что, задавшись ояреде-ленными температурой и давлением, можно определить равновесный состав паровой и жидкой фаз. Все три закона выведены для идеальных газов. [28]
Законность такого подхода требует некоторого пояснения, поскольку суммирование в равенстве (19.11) проводится по всем компонентам смеси. В случае единственной химической реакции это кажущееся затруднение мы преодолели, отметив, что для любого компонента смеси, который может считаться инертным, коэффициент v равен нулю. Теперь же мы имеем дело с компонентами, которые могут одновременно участвовать в двух реакциях и более. Таким образом, чтобы определить равновесный состав, мы в принципе должны найти те значения ( Т -, которые одновременно удовлетворяют уравнениям типа (19.25), записанным для каждого независимого стехиометрического уравнения. [29]
В этом методе, как и в элюентном анализе, малое количество пробы вводится в верхнюю часть колонки, насыщенной растворителем. Однако проба чистым растворителем не вымывается; вместо этого к растворителю добавляют вещество, сорбирующееся лучше любого компонента смеси. Этот хорошо адсорбирующийся компонент последовательно вытесняет компоненты анализируемой смеси и перемещает их по колонке. По предложению Тизелиуса вытесняющий реагент называют вытеснительным проявителем. Однако мы будем пользоваться термином вытеснитель, сохраняя термин проявитель для элюирующего агента, обусловливающего перемещение компонентов по колонке в виде разделенных полос. По внешнему виду кривая на рис. 66, а напоминает кривую фронтального анализа, так как представляет собой ряд ступеней с горизонтальными участками. Однако она существенно отличается от кривой фронтального анализа, так как каждая зона в случае вытеснительного проявления содержит лишь один компонент. Так как каждый компонент вытесняет все менее сорбируемые компоненты, различные растворенные вещества располагаются по зонам в соответствии с их адсорбционной способностью. [30]
Страницы: 1 2 3 4