Iva-группа
Cтраница 2
Своеобразно отношение простых веществ IVA-группы к кислотам. В ряду стандартных электродных потенциалов германий располагается между медью и серебром ( после водорода), а олово и свинец непосредственно перед водородом. [16]
Сравнивая свойства водородных соединений элементов IVA-группы нетрудно установить, что в ряду СН4 ( метан), SiH4 ( силан), СеИ4 ( герман) силан окисляется легче, чем метан и Герман, и в отличие от них вступает во взаимодействие с водой. [17]
Какие из элементов II1A - и IVA-групп в свободном состоянии являются полупроводниками. [18]
Какие из элементов IIIA - и IVA-групп в свободном состоянии являются полупроводниками. [19]
Иногда элементы подгруппы германия называют металлами IVA-группы. Формально в их число входит и сам германий. Однако, как известно, германий является типичным полупроводником с преимущественно ковалентной связью, а следовательно, металлом в свободном состоянии быть не может. Тем не менее в большом числе соединений с более электроотрицательными элементами германий выступает в качестве катионообразователя, что с химической точки зрения отражает металлическую природу элемента. [20]
Иногда элементы подгруппы германия называют металлами IVA-группы. [21]
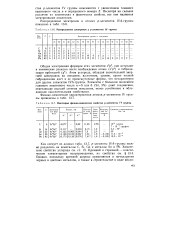 |
Распределение электронов у р-элементов IV группы.| Некоторые физико-химические свойства р-элементов IV группы. [22] |
Как следует из данных табл. 13.7, р-элементы IVA-группы можно разделить на неметаллы С, Si, Ge и металлы Sn и Pb. [23]
На каких подуровнях находятся валентные электроны у р-элементов IVA-группы. Какая степень окисления более характерна для германия, олова и свинца. [24]
Как следует из данных табл. 120, р-элементы IVA-группы можно разделить на неметаллы С, Si, Ge и металлы Sn и РЬ. [25]
В этой главе рассматриваются элементы трех групп периодической системы: IIIA-группы бора, IVA-группы углерода и группы VA - сурьма и висмут. Атомы их характеризуются застройкой электронами р-подуровня наружного уровня. У этих элементов, за исключением алюминия, восстановительная способность выражена сравнительно слабо. В свободном состоянии они характеризуются свойствами, отличающимися от свойств типичных металлов. Некоторые из соответствующих элементарных веществ ( кремний, германий) являются полупроводниками, иные ( бор, алмаз) отличаются большой твердостью. Значение в современной технике как элементарных веществ, так и некоторых соединений этих элементов очень велико. [26]
Металлы ША-группы ( Al, Ga, In, Tl), а также металлы IVA-группы ( Sn, Pb), т.е. все р-металлы, с кремнием соединений не образуют. Напротив, низшие силициды переходных металлов являются металлидами. В этом проявляется общая тенденция, отмеченная выше, - нарастание ковалентного вклада по мере увеличения содержания анионообразователя в формульной единице. [27]
Элементы подгруппы хрома при нагревании реагируют с галогенами, халько-генами, пниктогенами ( кроме висмута), неметаллами IVA-группы, бором. Кроме того, они реагируют с большинством металлов с образованием твердых растворов или интерметаллических соединений. [28]
Элементы подгруппы хрома при нагревании реагируют с галогенами, халькогенами, пниктогенами ( кроме висмута), неметаллами IVA-группы, бором. Кроме того, они реагируют с большинством металлов с образованием твердых растворов или интерметаллических соединений. Таким образом, в химическом отношении хром и его аналоги, несмотря на кажущуюся инертность, обусловленную пассивирующим действием оксидных пленок, относятся к довольно активным металлам. [29]
Элементы подгруппы хрома при нагревании реагируют с галогенами, халько-генами, пниктогенами ( кроме висмута), неметаллами IVA-группы, бором. Кроме того, они реагируют с большинством металлов с образованием твердых растворов или интерметаллических соединений. [30]
Страницы: 1 2 3 4