Положительный конец - диполе
Cтраница 3
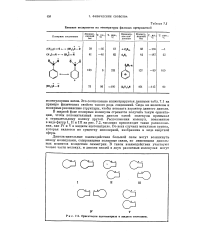 |
Ориентация ацетонитрила в жидком состоянии. [31] |
В жидкой фазе полярные молекулы стремятся получить такую ориентацию, чтобы положительный конец диполя одной молекулы примыкал к отрицательному полюсу другой. Расположения молекул, показанные в виде фигур I, II и III на рис. 7.2, численно превосходят такие расположения, как IV и V в жидком ацетонитриле. Во всех случаях метильная группа, которая является по существу неполярной, изображена в виде инертной сферы. [32]
Присоединение НОХ происходит по электрофильному механизму с первоначальной атакой атомом галогена - положительным концом диполя НОХ. В соответствии с правилом Мар-ковникова положительный галоген присоединяется к тому атому углерода двойной связи, с которым соединено большее число атомов водорода. Получающийся карбокатион ( либо ион бро-мония или иодония) взаимодействует с ОН или с водой, давая продукт. [33]
 |
Некоторые характеристики пятичленных гетероциклов. [34] |
Есть основания утверждать, что, поскольку гетероатом является донором двух р-электронов, положительный конец диполя находится на нем, а диеновая часть молекулы обогащается электронами. Это является одной из причин большей реакционной способности ( по сравнению с бензолом) фурана, пиррола и тиофена в реакциях электрофильного замещения. Кроме того, так как у всех пятичленных ароматических гетероциклов энергия сопряжения меньше, чем у бензола, образование ими о-комплексов с электрофильными реагентами происходит легче. [35]
Есть основания утверждать, что, поскольку гетброатом является донором двух р-элсктронов, положительный конец диполя находится на нем, а диеновая часть молекулы обогащается электронами. Это является одной из причин большей реакционной способности ( по сравнению с бензолом) фурана, пиррола и тиофенэ в реакциях электрофильного замещения. Кроме того, так как у всех пятичленных ароматических гетероциклов энергия сопряжения меньше, чем у бензола, образование ими о-комплексов с электрофильными реагентами происходит легче. [36]
Сопоставляя полученные величины с экспериментальными, приходим к выводу, что для обеих групп положительный конец диполя направлен к ароматическому ядру. Несмотря на большую электроотрицательность кислорода, дипольный момент тиоизоциа-натной группы имеет большее значение. [37]
 |
Шкала электроотрицательности Полинга. [38] |
Углерод, связанный с элементами, расположенными на шкале вправо от него, оказывается положительным концом диполя, в связях с элементами, расположенными левее, - отрицательным концом диполя. [39]
Она осуществляется в результате атаки атомом кислорода воды атома С карбонильной группы, который является положительным концом диполя, образуемого полярными связями с кислородом, и поэтому несет небольшой положительный заряд. [40]
Далее, на стадии роста цепи анионный заряд поляризует я-связь молекулы стирола таким образом, что положительный конец диполя присоединяет инициированный мономер. [41]
Это приводит к выводу, что в этих случаях атом галогена вследствие электроно-донорного эффекта может стабилизировать положительный конец диполя в структуре А. [42]
В основе этой реакции лежит атака атома кислорода воды на атом С карбонильной группы, который является положительным концом диполя, образуемого полярными связями с кислородом, и поэтому несет небольшой положительный заряд. [43]
Положительное значение адсорбционного - потенциала указывает на то, что молекулы органического вещества обращены к поверхности ртути положительным концом диполя. Другие органические вещества могут быть обращены к поверхности ртути отрицательным концом диполя, что приведет к сдвигу максимума электрокапиллярной кривой в сторону отрицательных потенциалов. [44]
Это едва ли можно объяснить исключительно большим моментом ковалентной структуры, так как при этом иод был бы положительным концом диполя, а не отрицательным, каким он, повидимому, является. В то же время в газообразной молекуле хлористого калия наблюдаемый момент оказывается неожиданно мал, хотя в этом случае скорее, чем где бы то ни было, следовало ожидать, что связь будет полностью ионной. Эти примеры иллюстрируют трудности, встречающиеся при использовании подобных расчетов, и некоторую неуверенность в объяснении результатов, полученных таким путем. [45]
Страницы: 1 2 3 4