Константа - электролитическая диссоциация - кислота
Cтраница 1
Константа электролитической диссоциации кислоты К при данных условиях постоянна, поэтому согласно уравнению ( 7) определение концентрации ионов зависит только от отношения концентраций кислоты и соли, взятых для приготовления буферной смеси, и не зависит от абсолютного значения концентраций. Вследствие этого при разбавлении буферного раствора концентрация водородных ионов должна оставаться неизменной. [1]
Константа электролитической диссоциации кислоты / С при данных условиях постоянна, поэтому согласно уравнению ( 6) определение концентрации ионов зависит только от отношения концентраций кислоты и соли, взятых для приготовления буферной смеси, и не зависит от абсолютного значения концентраций кислоты и соли. Вследствие этого при разбавлении буферного раствора концентрация водородных ионов должна оставаться неизменной. [2]
Константа электролитической диссоциации кислоты НАп, определяемая обычными методами ( Коб. [3]
Величина / С ( константа электролитической диссоциации кислоты) при данных условиях постоянна, поэтому значение концентрации водородных ионов будет определяться отношением концентраций кислоты и соли, взятых для приготовления буферной смеси. [4]
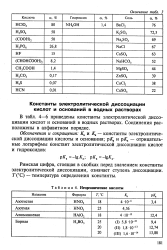
В табл. 85 - 87 приведены константы электролитической диссоциации кислот и оснований в водных растворах. Соединения расположены в алфавитном порядке. [5]
 |
Степень электролитической диссоциации важнейших электролитов в 0 1 н. растворах.| Неорганические кислоты. [6] |
В табл. 72 - 74 приведены константы электролитической диссоциации кислот и оснований в водных растворах. Соединения расположены в алфавитном порядке. [7]
 |
Неорганические кислоты. [8] |
В табл. 4 - 6 приведены константы электролитической диссоциации кислот и оснований в водных растворах. Соединения расположены в алфавитном порядке. [9]
Растворимость малорастворимой соли в кислоте тем больше, чем меньше константа электролитической диссоциации кислоты, анионы которой входят в состав данной соли. [10]
Растворимость малорастворимой соли в кислоте тем больше, чем меньше константа электролитической диссоциации кислоты, анионы которой входят в состав данной соли. Другими словами, чем больше растворимость данного электролита в воде и чем слабее кислота, образующая его, тем больше этот электролит растворяется в кислоте. [11]
Ю-4, то есть приблизительно в десять раз больше; константа электролитической диссоциации р-оксипропио-новой кислоты равна 3 X Ю-5 то есть всего в два с небольшим раза больше, чем пропионовой. Отсюда видно, что спиртовый гид-роксил, соседний с карбоксилом, оказывает наибольшее влияние. Простейшая оксикислота - гликолевая, на ней можно рассмотреть типичные для оксикислот свойства. Как кислота, она дает многочисленные ооли и разнообразные эфиры, в образовании которых принимают участие спирты, с которыми вступает в реакцию гликолевая кислота. Как спирт, гликолевая кислота дает простые и сложные эфиры. [12]
Растворимость малорастворимой соли в кислоте, тем больше, чем меньше константа электролитической диссоциации кислоты, анионы которой входят в состав данной соли. [13]
Кроме того, растворимость трудно растворимой соли тем больше, чем меньше константа электролитической диссоциации кислоты, анионы которой входят в состав данной соли. Так, в уксусной кислоте СаС О4 ( / Сшс о, 5 9 - 10 - 2) не растворяется, а карбонат кальция ( ПРСасоэ1 7 - 10 - 8; / С ] н соа 4 13 - К) -) растворяется. [14]
Употребляя при калибровке электрода буферную смесь с кислотой, константа электролитической диссоциации которой близка к константе электролитической диссоциации кислоты испытуемого раствора и рН близко к рН испытуемого раствора, можно свести ошибку опыта к очень малым величинам. [15]
Страницы: 1 2