Константа - протолитическая диссоциация
Cтраница 2
 |
Спектр поглощения аспирина при различных рН. [16] |
Гальбан и Кортюм [13] указывают, что для определения констант протолитической диссоциации возможно применение любого оптического метода, лишь бы наблюдалось различие в соответствующих свойствах не-диссоциированной кислоты и ее аниона. [17]
Вандерзее и Кунст [95] установили, что минимальная ошибка в определении констант протолитической диссоциации с помощью индикатора достигается при условии, если показатели констант диссоциации кислоты и индикатора отличаются друг от друга приблизительно на единицу. Использование кислотно-основных индикаторов позволяет применять спектрофотометры со стеклянной оптикой. [18]
Изложенные выше представления явились основой разработанного рядом исследователей [21-30] спектрофотометрического метода определения констант протолитической диссоциации, в частности, диссоциации кислотно-основных индикаторов. [19]
В соответствии с принятыми обозначениями MII - ступенчатая константа устойчивости комплекса двухвалентного железа FeA 1, а и 1 - ступенчатая константа устойчивости комплекса трехвалентного железа FeA2; Pi2, Pin, Рзв2, Pis - общие константы устойчивости комплексов Fe ( III) составов FeAt, FeAOH, Fe3Ae ( OH) J и FeA3; Ka - константа протолитической диссоциации кислоты НА; Ю1 - [ FeOH ] fe / [ Fe3 l - константа гидролиза. [20]
Для расчета констант ассоциации металла с полиэлектролитом важно знать константы диссоциации полимера по кислотному механизму. Однако константы протолитической диссоциации очень сильно зависят от ионной силы раствора и плотности заряда на цепи полиэлектролита. В присутствии ионов металла может измениться конформация цепи, что вызовет в свою очередь изменение плотности заряда; кроме того, присоединение ионов с разным положительным зарядом ( одно и / или двухза-рядных) к одной стороне цепи по-разному влияет на изменение плотности заряда на других участках цепи. [21]
Спектрофотометрическое определение констант протолитической диссоциации ализарина S не представляет трудности, поскольку эти величины существенно отличаются друг от друга ( см. табл. IV. Нахождение констант протолитической диссоциации лейкоализарина спектрофотометрическим методом представляет собой значительно более сложную задачу. [22]
Аналогичная картина наблюдается и в случае лейкоализаринатных комплексов. Сопоставление величин констант протолитической диссоциации ализаринатных и лейкоализаринатных комплексов к констант диссоциации лейкоализарина S и его лейкоформы показывает усиление кислотных свойств протоногенных групп координированных анионов красителя и лейкокрасителя. [23]
 |
Кислотно-основные индикаторы ( водные растворы. [24] |
Этот набор индикаторов охватывает почти всю шкалу рН и позволяет проводить как определение рН, так и кислотноос-новное титрование. Индикаторы используют также при определениях констант протолитической диссоциации неокрашенных кислот. [25]
Кларка в отношении повышения термодинамической строгости, большего удобства интерпретации экспериментальных данных и большей точности в определении констант протолитической диссоциации. [26]
В противоположность окислительно-восстановительным про-дессам, для характеристики которых применяется окислительный потенциал, сила кислот и оснований оценивается обычно с помощью константы протолитической диссоциации, а не кислотного потенциала. [27]
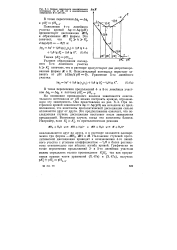 |
Кривые зависимости окислительного потенциала Аф от рН ( / и окислительного напряжения I от рН ( 2. [28] |
При построении кривой зависимости Аф Аф ( рН) мы исходили из предположения, что константы протолитической диссоциации сильно отличаются друг от друга. Это предположение означает, что последующая ступень диссоциации наступает после завершения предыдущей. Возможны случаи, когда эти константы близки. [29]
По кривым частной зависимости ф / ( рСа) мо жно установш ь число координируемых групп А, но число одновременно связываемых в комплекс протонов, которое определяет вид лиганда, остается неизвестным. Для многоосновной кислоты со значительно различающимися ступенчатыми константами протолитической диссоциации ( не менее, чем на 2 порядка) можно, создав определенную кислотность, добиться доминирования той или иной ионизированной формы кислоты. И в этом случае функция ф / ( рСа) практически будет означать зависимость окислительного потенциала системы от концентрации этой формы. Однако необходимо учитывать возможность диссоциации протонированного лиганда в комплексе под влиянием поляризующего действия иона металла. Лимонная кислота характеризуется достаточно близкими значениями констант протолитической диссоциации, поэтому определить состав протониро-ванных комплексов с помощью зависимости ф / ( рСа) не удается. [30]
Страницы: 1 2