Константа - кислота
Cтраница 1
Константы кислоты / Са ( НзО) и основания Кб ( ОН -) требуют особого обсуждения. [1]
Сравнение констант кислот, выделенных указанными методами, показывает, что омыление оксидата 1 н раствором КОН в диэтиленгликоле дает более высококачественные нафтеновые кислоты. [2]
В действительности константы кислот несколько ниже, чем солей с неорганическими катионами или солей четвертичных аммониевых оснований, но близки к константам солей моно -, ди - и тризамещенных аммониевых оснований, содержащих водород, способный к образованию водородной связи. Это уменьшение р / ( происходит за счет образования водородной связи между ионами. Величины рК других сильных кислот в этом же растворителе невелики и сильно дифференцированы. [3]
При сопоставлении приведенных выше констант диссоциацш кислот с нормальной цепью видно, что по мере удлинения цет константа сначала снижается, при переходе от пропионовой к мае ляной возрастает, а затем снова несколько уменьшается. [4]
ОН, а не от константы кислот - ности иона Н30 или константы основности молекулы Н20, как это имеет место в случае незаряженных или анионных кислот. [5]
Эта цепь ничем не отличается от той, которую применяют при определении констант кислот. [6]
Апротонные растворители не способны отщеплять протоны, поэтому для них невозможно определить константу кислоты. [7]
Улучшение условий титрования может быть достигнуто, если при переходе к не-всдному растворителю константа кислоты уменьшается в меньшей степени, чем произведение ионов среды. [8]
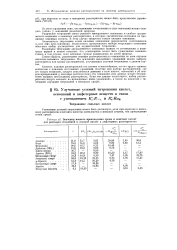 |
Значение ионного произведения среды и констант кислот для растворов бензойной и соляной кислот в амфотерных растворителях. [9] |
Улучшение условий титрования может быть достигнуто, если при переходе к неводному растворителю константа кислоты уменьшается в меньшей степени, чем произведение ионов среды. [10]
Эта: цепь ничем не отличается от той, которую применяют при определении констант кислот. [11]
Для определения констант К0бА и С0бв применяются те же самые цепи, что и для определения констант кислот и оснований. [12]
Как мы видели, улучшение условий титрования можег быть достигнуто, если при переходе к неводному растворителю константа кислоты уменьшается в меньшей степени, чем произведение ионов среды. [13]
 |
Кривые титрования водных растворов уксусной кислоты ( CQ - 10 - 1 моль / л, СоЮ 3 моль / л растворами щелочей такой же концентрации. [14] |
В формулах, с помощью которых вычисляют рН в различных точках кривых титрования, содержатся константы автопротолиза растворителей и константы кислот протолитических пар. Зависимость значений этих констант от температуры определяет зависимость рЫ раствора от температуры. [15]
Страницы: 1 2 3