Константа - нестойкость - комплексный ион
Cтраница 3
Таким образом, состояние изучаемой системы будет определяться константами нестойкости комплексных ионов РЗЭ и ЭДТА, которые имеют малые значения. [31]
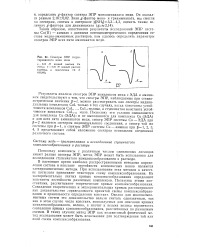 |
Спектры ЭПР гидра-тированного иона меди. [32] |
В настоящее время наиболее распространенными методами определения состава и констант нестойкости комплексных ионов являются электрохимические методы. При использовании этих методов в качестве постулата принимают некоторую схему комплексообразования. Из экспериментально снятых кривых комплексообразования определяют константы нестойкости различных комплексов. Пользуясь этими константами, рассчитывают теоретические кривые комплексообразования. Совпадение теоретических и экспериментальных кривых рассматривают как доказательство справедливости принятой схемы комплексообразования и правильности определения констант. Однако для многокомпонентных систем это доказательство нельзя считать однозначным, так как в этом случае число констант, используемых для описания кривых комплексообразования, велико, а значит и весьма велика вероятность совпадения кривых комплексообразования, рассчитанных по различным схемам. В таких случаях метод ЭПР как независимый физический метод исследования может быть использован для подтверждения той или иной схемы комплексообразования. [33]
Величина К отношение произведения концентрации продуктов диссоциации комплексного иона к концентрации комплексного иона) называется константой нестойкости комплексного иона. Чем больше константа, тем менее устойчив комплекс. Величины констант нестойкости комплексных ионов приведены в табл. 14 на стр. [34]
Метод амперометрического титрования позволяет изучать некоторые комплексные соединения, в частности определять число лигандов и величину константы нестойкости комплексного иона. [35]
Величина К ( отношение произведения концентрации продуктов диссоциации комплексного иона к концентрации комплексного иона) называется константой нестойкости комплексного иона. Чем больше константа, тем менее устойчив комплекс. [36]
Наоборот, если произведение растворимости осадка, содержащего ион, который входит в состав комплекса, значительно меньше константы нестойкости комплексного иона, последний может быть разрушен и его комплексообразователь войдет в состав осадка. Для окончательного решения вопроса о направлении реакции необходимо все же провести соответствующий расчет, так как концентрации ионов и молекул в уравнение константы нестойкости часто входят в соответствующих степенях, и верное решение вопроса о направлении процесса дает только вычисление. Так, например, произведение растворимости AgCl, равное 1 56 - 10 - 10, меньше константы нестойкости комплексного иона [ Ag ( NH3) 2 ], равной 6 8 - 10 - 8, но все же осадок AgCl в аммиаке растворяется. [37]
Ответ мотивировать и проверять по таблице ( см. Приложение, табл. 12) совпадает ли он с соотношением констант нестойкости соответствующих комплексных ионов. [38]
Ответ мотивировать и проверить по таблице ( см. Приложение, табл. 13) совпадает ли он с соотношением констант нестойкости соответствующих комплексных ионов. [39]
Величина / С ( отношение произведения концентрации продуктов диссоциации комплексного иона, к концентрации комплексного иона) называется константой нестойкости комплексного иона. Чем больше константа, тем менее устойчив комплекс. [40]
Такое действие рассматриваемых реагентов ( KCI, KI и H2S) находится в прямой зависимости от растворимости образующихся соединений и констант нестойкости комплексных ионов. [41]
Страницы: 1 2 3