Константа - нестойкость - комплекс
Cтраница 1
Константа нестойкости комплекса является величиной постоянной; если разбавление сравниваемых растворов производить раствором реактива постоянной концентрации, то и [ R ] тоже будет величиной постоянной. [1]
Константа нестойкости комплекса ( комплексного иона) характеризует прочность ( устойчивость) внутренней сферы комплексного соединения. [2]
Константа нестойкости комплекса Na3 [ Ag ( S2O j) 2l составляет 4 - 10 - 14, ч потому равновесие его диссоциации нарушить значительно труднее, чем в случае аммиаката серебра. [3]
Константа нестойкости комплекса Na3 [ Ag ( S2O3) 2 ] составляет 4 1 ( Н4, а потому равновесие его диссоциации нарушить значительно труднее, чем в случае аммиаката серебра. [4]
Константа нестойкости комплекса Na3 [ Ag ( 8203) 2 ] составляет 4 10 - u, a потому равновесие его диссоциации нарушить значительно труднее, чем в случае аммиаката серебра. [5]
Константа нестойкости комплекса Nas [ Ag ( S2Os) 2 ] составляет 4 - 10 -, потому равновесие его диссоциации нарушить значительно труднее, чем в случае аммиаката серебра. [6]
Константу нестойкости комплекса [ VOCH3CHOCOO ], образованного за счет водорода гидроксильной группы, рассчитать нельзя, так как неизвестна константа кислотной диссоциации спиртовой группы. [7]
Если константа нестойкости комплекса мала, то изменение концентраций веществ при титровании и вид кривых титрования будет подобным тем, которые получаются в случае реакции осаждения. [8]
Для константы нестойкости комплекса Co ( SCN) [371] приводится еще другая величина, равная 0 061 при нулевой ионной силе раствора. [9]
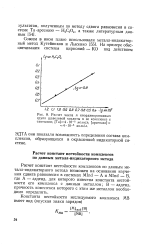 |
Расчет числа п координированных. [10] |
Расчет констант нестойкости комплексов по данным металл-индикаторного метода возможен на основании изучения сдвига равновесия в системах Mind - Аи Mind - В, где А - адденд, для которого известна константа нестойкости его комплекса с данным металлом; В - адденд, прочность комплекса которого с этим же металлом необходимо определить. [11]
Измерение констант нестойкости комплексов с этими аддендами показывает, что максимальной устойчивостью обладают производные этилендиаминтетрауксусной кислоты, содержащие замкнутые на азот пятичленные циклы. По мере увеличения п устойчивость комплексов уменьшается. [12]
Величины констант нестойкости комплексов позволяют судить о направлении химического процесса: реакция пойдет в сторону образования комплекса с меньшей константой нестойкости, что равноценно большей константе устойчивости. Этим широко пользуются в аналитической химии при создании условий эффективного разделения ионов М и анионов. [13]
Значения константы нестойкости комплекса Ри -, полученные различными авторами, находятся в удовлетворительном согласии. Небольшое расхождение их обусловлено в некоторой мере различием ионной силы исследуемых растворов. Поскольку Формэн и Смит ( см. стр. Ри ( III) при рН3 3, когда, по данным других авторов [49,50], существует в основном комплексный ион Рну -, образование водородсодержащего комплекса ими не наблюдалось. [15]
Страницы: 1 2 3 4