Константа - нестойкость - комплекс
Cтраница 2
Величина константы нестойкости комплекса RsZn была определена нами также по данным флуориметрического определения состава комплекса. [16]
Значения констант нестойкости ЭДТА комплексов редкоземельных элементов, найденные авторами потенциометрическим методом, приведены ниже. [17]
 |
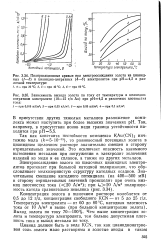
Оптическая плотность изомоляр-ной серии растворов. Образование. а прочного комплекса МАП. б непрочного комплекса МАгс. [18] |
О константе нестойкости комплекса можно судить по форме кривой состав - свойство, по отношению к разбавлению раствора такого состава, который отвечает максимуму на кривой состав - свойство. [19]
Чем меньше константа нестойкости комплекса, тем более прочен комплекс. [20]
Чем меньше константа нестойкости комплекса, тем более прочен комплекс. [21]
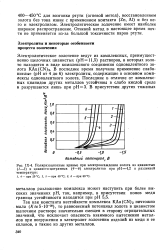 |
Поляризационные кривые при электроосаждении золота из цианистых ( 1 - 3 и цианисто-цитратных ( 4 - 6 электролитов при рН 4 2 и различной температуре. [22] |
Так как константа нестойкости комплекса KAu ( CN) 2 ничтожно мала ( / ( 5 - Ю-39), то равновесный потенциал золота в цианистом щелочном растворе значительно смещен в сторону отрицательных значений, что исключает опасность взаимного вытеснения металлов при погружении в электролит золочения изделий из меди и ее сплавов, а также из других металлов. [23]
К - константа нестойкости комплекса ML; v - заряд М; р - заряд L; индекс s относится к концентрации лиганда-катализатора на границе диффузионного слоя и двойного электрического слоя; k, k2, k / - кинетические параметры. [24]
Так как константа нестойкости комплекса KAu ( CN) 2 ничтожно мала ( & 5 - 10 - 39), то равновесный потенциал золота в цианидном щелочном растворе значительно смещен в сторону отрицательных значений. Это исключает опасность взаимного вытеснения металлов при погружении в электролит золочения изделий из меди и ее сплавов, а также из других металлов. [26]
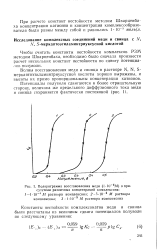
Чтобы считать константы нестойкости комплексов РЗМ методом Шварцеибаха, необходимо было сначала произвести расчет нескольких констант нестойкости по сдвигу потенциалов полуволн. [28]
Прецизионное определение констант нестойкости комплексов часто связано с большими экспериментальными трудностями и требует значительной затраты времени. Особенно это относится к изучению комплексных соединений элементов со степенью окисления 4 и больше, которые подвергаются в водных растворах сильному гидролизу и проявляют повышенную склонность к образованию гидролитических полиядерных соединений. Между тем, для решения конкретных аналитических задач часто возникает необходимость в получении более широких, хотя и менее точных, данных о прочности комплексных соединений в растворах. Во многих случаях химика-аналитика вполне удовлетворяют сведения об относительной прочности комплексов одного элемента с различными лигандами или ряда катионов металлов с одним и тем же лигандом. Часто возникает необходимость в быстрой оценке маскирующего действия комплексообразующих реагентов. В таких случаях может быть весьма полезным металл-индикаторный метод, различные варианты которого описаны в этой книге. [29]
Для расчета констант нестойкости комплексов был использован метод кривых относительного поглощения. Установлено, что все аминокислоты образуют с ионами Ри ( III) достаточно прочные комплексные соединения. Различие в поведении этих аминокислот в водных растворах объясняется наличием в их составе разных кольцевых структур. Бензольное кольцо фе-нилаланина и тирозина в комплексообразовании не участвует. [30]
Страницы: 1 2 3 4